- N-Allylanilin
-
Strukturformel 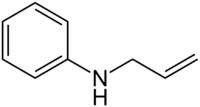
Allgemeines Name N-Allylanilin Andere Namen - N-(2-propenyl)anilin
- 3-(N-phenylamino)propen
- N-Allyl-N-phenylamin
- N-2-Propenylanilin
- N-Phenylallylamin
- N-Allylbenzolamin
Summenformel C9H11N CAS-Nummer 589-09-3 PubChem 68525 Kurzbeschreibung farblose Flüssigkeit[1]
Eigenschaften Molare Masse 133,19 g·mol−1 Aggregatzustand flüssig
Dichte 0,98 g·cm−1 (20 °C)[2]
Schmelzpunkt Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Achtung
H- und P-Sätze H: 302-312-315-319-332-335 EUH: keine EUH-Sätze P: 261-280-305+351+338 [1] EU-Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 20/21/22-36/37/38 S: 26-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. N-Allylanilin ist eine organische Verbindung. Sie besteht aus einem Anilingerüst, welches eine Allylgruppe am Stickstoffatom trägt.
Darstellung
N-Allylanilin kann durch Alkylierung von Anilin mit Allylchlorid[3], -bromid[4] oder -iodid[5] hergestellt werden. Auch die Synthese durch eine Ullmann-Aminierung aus Allylamin und Phenyliodid ist bekannt.[6]
Historisch führte N-Allylanilin zur Strukturaufklärung von Chinolin, welches 1880 unter Verwendung von Bleioxid aus N-Allylanilin synthetisiert werden konnte.[7]
Einzelnachweise
- ↑ a b c d e Datenblatt N-Allylaniline bei Sigma-Aldrich, abgerufen am 12. April 2011.
- ↑ Datenblatt N-Allylanilin bei Acros, abgerufen am 17. Juli 2010.
- ↑ H. Oehme, R. Thamm: Synthese und Reaktionsverhalten der (3-Aminopropy1)-phenylphosphine, in: J. Prakt. Chem 1973, 315, 526–538; doi:10.1002/prac.19733150320.
- ↑ F. L. Carnahan, C. D. Hurd: Pyrolysis pf Allylanilines, in: J. Am. Chem. Soc 1930, 52, 4586–4595; doi:10.1021/ja01374a062.
- ↑ V. Pace, F. Martinez, M. Fernandez, J. V. Sinisterra, A. R. Alcantara: Effective Monoallylation of Anilines Catalyzed by Supported KF, in: Org. Lett. 2007, 9, 2661–2664; doi:10.1021/ol070890o.
- ↑ D. Ma, Q. Cai, H. Zhang: Mild Method for Ullmann Coupling Reaction of Amines and Aryl Halides, in: Org. Lett. 2003, 5, 2453–2456; doi:10.1021/ol0346584.
- ↑ W. Koenigs: Synthese des Chinolins aus Allylanilin, in: Chem. Ber. 1879, 12, 453; doi:10.1002/cber.187901201128.
Wikimedia Foundation.
