- Strontiumformiat
-
Strukturformel 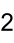
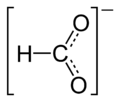
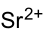
Allgemeines Name Strontiumformiat Summenformel C2H2SrO4 CAS-Nummer - 592-89-2 (Reinsubstanz)
- 6160-34-5 (Dihydrat)
PubChem 68967 Eigenschaften Molare Masse Aggregatzustand fest
Dichte Löslichkeit Sicherheitshinweise EU-Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Strontiumformiat ist das Strontiumsalz der Ameisensäure.
Herstellung
Strontiumformiat kann durch Reaktion von Strontiumcarbonat[4] oder Strontiumhydroxid mit Ameisensäure dargestellt werden.[2]
Eigenschaften
Strontiumformiat kristallisiert als Dihydrat im orthorhombischen Kristallsystem in der Raumgruppe D42 – P212121 und den Gitterparametern a = 730 pm, b = 1199 pm und c = 713 pm. In der Elementarzelle befinden sich vier Formeleinheiten.[1]
Das Dihydrat gibt zwischen 50 und 150 °C sein Kristallwasser ab.[4] Das Anhydrat kristallisiert ebenfalls im orthorhombischen Kristallsystem in der gleichen Raumgruppe wie das Dihydrat.[5] Die Gitterparameter betragen a = 687 pm, b = 874 pm und c = 727 pm. In der Elementarzelle befinden sich ebenfalls vier Formeleinheiten.[1]
Strontiumformiat zersetzt sich beim Erhitzen unter Bildung von Strontiumoxid.[4]
Einzelnachweise
- ↑ a b c Jean D'Ans, Ellen Lax: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-5406-0035-0, S. 744f. (Eingeschränkte Vorschau in der Google Buchsuche).
- ↑ a b c d R. Abegg, F. Auerbach: Handbuch der anorganischen Chemie, Verlag S. Hirzel, Bd. 2, 1908. S. 231; Volltext
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c A. Gonzalez, J. Jimenez, F. Rull: "On the kinetics of thermal decomposition of anhydrous strontium formate in vacuum" in Crystal Research and Technology 1985, 20(1), S. K11-K14. doi:10.1002/crat.2170200130
- ↑ N. R. McQuaker, K. B. Harvey: "Infrared and Raman Spectra of Single Crystals of Anhydrous Strontium Formate" in Canadian Journal of Chemistry 1972, 50(10), S. 1453 - 1460. doi:10.1139/v72-231
Kategorien:- Strontiumverbindung
- Formiat
Wikimedia Foundation.


