- Danaparoid
-
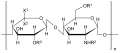
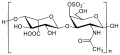
Strukturformel Mischpolymer aus Heparansulfat, Dermatansulfat und Chondroitinschwefelsäure Allgemeines Name Danaparoid Andere Namen - Danaparoid natrium
- Latein: Danaparoidum natricum
- Glycosaminoglycuronaanpolysulfat
CAS-Nummer - 308068-55-5
- 57459-72-0 (Danaparoid natrium)
ATC-Code B01AB09
Kurzbeschreibung weißes bis fast weißes, hygroskopisches Pulver[1] Arzneistoffangaben Wirkstoffklasse Verschreibungspflichtig: ja Monomer Monomer nicht angebbar, da Stoffgemisch Summenformel nicht angebbar, da Stoffgemisch Molare Masse ca. 6 kDa Eigenschaften Löslichkeit leicht löslich in Wasser [1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze Gefahrstoffkennzeichnung [1]
Danaparoid·Natrium
Xn
Gesundheits-
schädlichR- und S-Sätze R: 20-42/43 S: 22-36/37-38-45 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Danaparoid-Natrium, (Handelsname Orgaran®, Hersteller: Essex Pharma) ist ein Arzneistoff aus der Gruppe der Heparinoiden, der die Blutgerinnung – ähnlich wie Heparin – hemmt. Er besteht aus einer Mischung von Glykosaminoglykanen, welche aus Schweinedarmmukosa gewonnen werden. Die durchschnittliche molare Masse beträgt etwa 6 kDa.
Inhaltsverzeichnis
Zusammensetzung
Der Arzneistoff besteht hauptsächlich aus Heparansulfat (Suleparoid-Natrium, ca. 84 %). Darüber hinaus enthält Danaparoid-Natrium Dermatansulfat (Natriumsalz von Chondroitinsulfat B, ca. 12 %) und zu einem kleinen Anteil Chondroitinschwefelsäure (Chondroitinsulfat als freie Säure, ca. 4 %).[3]
Nur 4 % der Heparansulfatmoleküle besitzen eine hohe Bindungsaffinität zu Antithrombin III. Obwohl Danaparoid, ähnlich wie Heparin, aus Schweinedarmmukosa gewonnen wird, enthält das Gemisch keine Heparinfraktion.
Anwendung
Es wird zur Vorbeugung der tiefen Venenthrombose in Situationen gegeben, in denen Heparin nicht angewendet werden soll. Das sind meistens Patienten, bei denen durch Heparin ein Mangel an Blutplättchen verursacht wird, die sogenannte Heparin-induzierte Thrombozytopenie Typ II (HIT II).[4][5]
Gegenanzeigen
Nicht oder nur nach Abwägung darf es angewendet werden bei Personen, die bereits unter einer Blutungsneigung, unkontrolliert hohem Blutdruck, schwerer Nieren- oder Leberinsuffizienz, Magen- bzw. Zwölffingerdarmgeschwüren oder Hirnblutung leiden. Die Wirkung wird durch Gerinnungstests wie Prothrombinzeit gemessen. Diese können bis zu 5 Stunden nach Danaparoid-Injektion unzuverlässige Ergebnisse liefern. Bei schweren Blutungen kann die Wirkung durch Transfusion von frisch eingefrorenem Plasma gemindert werden. Eine regelmäßige Überprüfung der Anzahl der Blutplättchen ist notwendig.
Siehe auch
- Antikoagulation
- Hämostase
- Thrombus (Blutgerinnsel)
Einzelnachweise
- ↑ a b c d Datenblatt DANAPAROID SODIUM CRS beim EDQM, abgerufen am 7. Juni 2008.
- ↑ Datenblatt Heparan sulfate fast-moving fraction sodium salt from porcine intestinal mucosa bei Sigma-Aldrich, abgerufen am 28. April 2011.
- ↑ Thieme Chemistry (Hrsg.): Eintrag zu Danaparoid-Natrium im Römpp Online. Version 3.14. Georg Thieme Verlag, Stuttgart 2011, abgerufen am 18. März 2011.
- ↑ Elizabeth M. Van Cott, MD Massachusetts General Hospital Boston MA:New Anticoagulants and Heparin-Induced Thrombocytopenia(PDF).
- ↑ Greinacher, A.: Heparininduzierte Thrombozytopenie Dtsch. Ärztebl. 2003; 100: A 2220–2229 (Heft 34–35).
Weblinks
- Full label information for ORGARAN™ (Danaparoid-Sodium). Food and Drug Administration, 26. Juni 2001, S. 18, abgerufen am 5. Oktober 2010 (PDF (566 KB), englisch).
- Glykosaminoglykane bei Vetpharm UniZH

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-B01
- Gesundheitsschädlicher Stoff
- Sensibilisierender Stoff
- Biopolymer
- Polysaccharid
- Copolymer
- Arzneistoff
- Antikoagulans
- Stoffgemisch
Wikimedia Foundation.