- Dimethylbenzole
-
Xylole Name o-Xylol m-Xylol p-Xylol Andere Namen 1,2-Dimethylbenzol 1,3-Dimethylbenzol 1,4-Dimethylbenzol Strukturformel 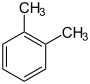

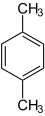
CAS-Nummer 95-47-6 108-38-3 106-42-3 1330-20-7 (Isomerengemisch)[1] PubChem 7237 7929 7809 Summenformel C8H10 Molare Masse 106,17 g·mol−1 Aggregatzustand flüssig Kurzbeschreibung farblose Flüssigkeit Schmelzpunkt −25,2 °C[2] −48 °C[3] 13,3 °C[4] Siedepunkt 144 °C[2] 139 °C[3] 138 °C[4] Löslichkeit unlöslich in Wasser Gefahrstoff-
kennzeichnung
[5]
Gesundheits-
schädlich(Xn) R-Sätze 10-20/21-38 S-Sätze (2)-25 Die Xylole (von griechisch ξύλον (xýlon) = „Holz“) (korrekterweise Xylene oder nach der IUPAC-Nomenklatur Dimethylbenzene) sind aromatische Kohlenwasserstoffe mit der allgemeinen Summenformel C8H10. Sie bestehen aus einem Benzolring mit zwei Methylsubstituenten (–CH3). Durch unterschiedliche Anordnung der Methylgruppen ergeben sich drei Konstitutionsisomere des Xylols: 1,2-Xylol (ortho-Xylol), 1,3-Xylol (meta-Xylol) und 1,4-Xylol (para-Xylol). In der Technik (z.B. als Lösemittel) werden sie meist als (ungetrenntes) Isomerengemisch verwendet und setzen sich in der Regel aus 60 % m-Xylol, 10–25 % o-Xylol und 10–25 % p-Xylol zusammen. Als Lösemittel verwendete Xylolmischungen enthalten häufig auch Ethylbenzol, das im gleichen Temperaturbereich siedet und ähnliche Lösungseigenschaften besitzt.
Inhaltsverzeichnis
Eigenschaften
Xylole sind farblose Flüssigkeiten, die kaum in Wasser löslich sind (0,2 g/l). In Ethern, Alkoholen, Benzol und Aceton zeigen sie jedoch gute Löslichkeit. Wässrige Lösungen zeigen schon im Konzentrationsbereich von 0,53 bis 1,8 ppm einen erkennbaren Geschmack. Xylole haben typische aromatische Gerüche; die Geruchsschwelle liegt bei 0,2 und 174 mg/m3. Die Siedepunkte der drei Isomere liegen nah beieinander, während ihre Schmelzpunkte sich deutlich unterscheiden. Das p-Xylol, das die höchste Symmetrie aufweist, besitzt den höchsten Schmelzpunkt. Die Dichte beträgt 0,86–0,88 g/cm3[1]; die Xylole sind also alle leichter als Wasser. Der Flammpunkt liegt bei etwa 30 °C (abhängig vom Isomer),[1] die Zündtemperatur zwischen 463 und 528 °C.[1] Sie verbrennen mit stark rußender Flamme.
Darstellung
Rohstoffquellen für die Gewinnung der Xylole sind Kohle (aus Steinkohlenteer) und Erdöl (durch Cracken), wobei Isomerengemische anfallen. Da die Isomere ähnliche Siedepunkte haben, ist eine Auftrennung durch Destillation schwierig. Die Abtrennung des o-Isomers wird technisch durch Rektifikation durchgeführt, anschließend kann p-Xylol aufgrund seines relativ hohen Schmelzpunktes durch Ausfrieren getrennt werden. Großtechnisch spielt die Abtrennung des p-Xylols mit Hilfe der Adsorption mit einem Molekularsieb eine wichtige Rolle.
Verwendung
Xylole finden als Lösungsmittel Verwendung und dienen zur Herstellung von Kunst- und Klebstoffen. Da der Flammpunkt von Xylol oberhalb von 21 °C liegt, ist es in der Praxis neben Butylacetat eines der wichtigsten Lösungsmittel für Lacke. Weiterhin werden sie Kraftstoffen zur Erhöhung der Oktanzahl beigemengt.
p-Xylol ist Ausgangsstoff für die Darstellung von Terephthalsäure (> 1 Million Jahrestonnen) und o-Xylol in ähnlichen Mengen zur Gewinnung von Phthalsäure für die Kunststoffindustrie. Durch Nitrierung erhält man die Nitroxylole, die durch anschließende Reduktion zur Darstellung der Xylidine dienen.
Neben dem Benzol und dem Toluol gehören die Xylole zu den technisch wichtigsten Aromaten, den so genannten BTEX-Aromaten.
Reaktionen
Die Methylgruppen (–CH3) können zu Carboxylgruppen oxidiert werden. Geeignete Oxidationsmittel zur Umsetzung beider Methylgruppen sind beispielsweise Kaliumpermanganat oder Chromschwefelsäure. o-Xylol wird so in Phthalsäure, m-Xylol in Isophthalsäure und p-Xylol in Terephthalsäure überführt. Durch Sauerstoff (z. B. in Gegenwart von Cobaltstearat als Katalysator) erhält man die entsprechenden Monocarbonsäuren, die Toluylsäuren (Methylbenzoesäuren). Xylole gehen die für Aromaten typischen Substitutionsreaktionen ein.
Gefahren
Xylole sind entzündlich und wirken gesundheitsschädigend bei Aufnahme über die Haut und die Atmungswege. Sie können zum Beispiel Kopfschmerzen, Gedächtnis- und Orientierungsstörungen hervorrufen. Xylole sind wassergefährdend (WGK 2).[1] Zwischen einem Luftvolumenanteil von 1 bis 8 % bilden sie explosive Gemische.[1] Emissionen von Xylolen sind hauptsächlich auf den Kfz-Verkehr zurückzuführen. In den letzten Jahren ist ein Rückgang der Xylolemissionen zu verzeichnen.
Einzelnachweise
- ↑ a b c d e f Eintrag zu CAS-Nr. 1330-20-7 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 16. März 2008 (JavaScript erforderlich).
- ↑ a b Eintrag zu CAS-Nr. 95-47-6 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 16. März 2008 (JavaScript erforderlich).
- ↑ a b Eintrag zu CAS-Nr. 108-38-3 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 16. März 2008 (JavaScript erforderlich).
- ↑ a b Eintrag zu CAS-Nr. 106-42-3 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 16. März 2008 (JavaScript erforderlich).
- ↑ Eintrag zu CAS-Nr. 1330-20-7 im European chemical Substances Information System ESIS.
Literatur
- Bewertung von Toluol- und Xylol-Immissionen. Erich Schmidt Verlag, Berlin (2000), ISBN 3-503-04071-4.
Weblinks
Wikimedia Foundation.
