- Eisen(II)-sulfid
-
Kristallstruktur 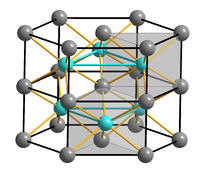
__ Fe2+ __ S2- Allgemeines Name Eisen(II)-sulfid Andere Namen Schwefeleisen
EisenmonosulfidVerhältnisformel FeS CAS-Nummer 1317-37-9 Kurzbeschreibung dunkelgraue oder schwarze, metallartige Stücke, Platten oder Stäbchen[1]
Eigenschaften Molare Masse 87,91 g·mol−1 Aggregatzustand fest
Dichte 4,84 g·cm−3[2]
Schmelzpunkt Löslichkeit praktisch unlöslich in Wasser[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 400 EUH: keine EUH-Sätze P: 273 [3] EU-Gefahrstoffkennzeichnung [2] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Eisen(II)-sulfid (alte Bezeichnung: Schwefeleisen) ist das Sulfid des zweiwertigen Eisens mit der Formel FeS.
Inhaltsverzeichnis
Eigenschaften
FeS ist unlöslich in Wasser. Mit Säuren reagiert es unter Bildung von Schwefelwasserstoff.
Beim Erhitzen auf höhere Temperaturen erfolgt bei 138 °C und 325 °C jeweils eine kristallographische Umwandlung im festen Zustand. [4]
Reines Eisen(II)-sulfid bildet hellbraune Kristalle. Die technische Ware ist meist durch Resteisen dunkel bis schwarz gefärbt.Herstellung
Sowohl im Labor als auch technisch lässt sich Eisen(II)-sulfid durch kurzes Erhitzen eines Gemisches aus Eisenpulver und Schwefelpulver in einer exothermen Reaktion herstellen:
Vorkommen
In der Natur findet sich Eisen(II)-sulfid als Pyrrhotin, Troilit und Mackinawit. [5]
Die bakterielle anaerobe Korrosion kann man durch die Schwarzfärbung durch Eisen(II)-sulfid erkennen, welches als Endprodukt entsteht. Dieser archaische Stoffwechsel der Bakterien spielt in der Eisen-Schwefel-Welt, einem Szenario für die frühe Evolution des Lebens, eine wichtige Rolle.
Verwendung
Eisen(II)-sulfid wurde früher für die Synthese der Schwefelsäure verwendet. Dabei wurde das Eisen(II)-sulfid unter Zufuhr von Luft geröstet, wobei das für die weitere Synthese benötigte Schwefeldioxid entstand. Im Labor kann Eisen(II)-sulfid zur Herstellung von Schwefelwasserstoff dienen.
Einzelnachweise
- ↑ a b Helmut Sitzmann, in: Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c Eintrag zu CAS-Nr. 1317-37-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 01.08.2007 (JavaScript erforderlich)
- ↑ a b Datenblatt Iron(II) sulfide bei Sigma-Aldrich, abgerufen am 29. März 2011.
- ↑ D'Ans-Lax, Taschenbuch für Chemiker und Physiker, Band 3 (1998), S.458; ISBN 3-540-60035-3
- ↑ Holleman, Wiberg, Lehrbuch der anorganischen Chemie (2007), S.1657; ISBN 978-3-11-017770-1
Kategorien:- Eisenverbindung
- Sulfid
Wikimedia Foundation.



