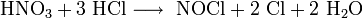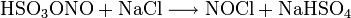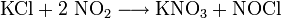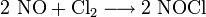- NOCl
-
Strukturformel 
Allgemeines Name Nitrosylchlorid Andere Namen Stickstoffoxichlorid, Nitrosoniumchlorid
Summenformel NOCl CAS-Nummer 2696-92-6 PubChem 17601 Kurzbeschreibung gelbes Gas, rote Flüssigkeit Eigenschaften Molare Masse 65,46 g·mol−1 Aggregatzustand gasförmig
Dichte 2,9831 kg·m−3 (0 °C)[1]
Schmelzpunkt −61,5 °C[1]
Siedepunkt −5,55 °C[1]
Dampfdruck 2,71 bar (20 °C)[1]
Löslichkeit in Wasser schnelle Hydrolyse[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 

Sehr giftig Ätzend (T+) (C) R- und S-Sätze R: 26-34-37 S: 26-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Nitrosylchlorid (NOCl) ist das Säurechlorid der Salpetrigen Säure HNO2. Es ist ein Nebenprodukt bei der Bildung von Königswasser. Die dabei entstehenden Chlorradikale vermögen die Edelmetalle Gold und Platin zu Tetrachloridogoldsäure bzw. Hexachloridoplatinsäure zu oxidieren:
Herstellung
Rohes Nitrosylchlorid entsteht bei der Umsetzung von konzentrierter Salpetersäure mit konzentrierter Salzsäure im Verhältnis 1:3 (Königswasser):
Zur Reindarstellung im Labor verwendet man einerseits die Reaktion von frischem Nitrosylhydrogensulfat mit wasserfreiem Natriumchlorid:
Andererseits erhält man es auch durch Einleitung von Stickstoffdioxid in eine Säule mit feuchtem Kaliumchlorid:
Zuletzt kann zur Herstellung auch Chlor bei −50 °C mit Stickstoffmonoxid gesättigt werden:[2]
Quellen
Wikimedia Foundation.