- Pentanatriumtriphosphat
-
Strukturformel 
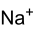

Allgemeines Name Pentanatriumtriphosphat Andere Namen - Natriumtripolyphosphat
- Natriumtriphosphat pentabasisch
Summenformel Na5P3O10 CAS-Nummer 7758-29-4 PubChem 517047 Kurzbeschreibung weißer, geruchloser Feststoff[1]
Eigenschaften Molare Masse 367,86 g·mol−1 Aggregatzustand fest
Dichte 2,52 g·cm−3[1]
Schmelzpunkt Löslichkeit löslich in Wasser: 145 g·l−1 (25 °C)[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze EU-Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 24/25 LD50 3120 mg·kg−1 (oral Ratte)[2]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Pentanatriumtriphosphat (auch Natriumtripolyphosphat) ist ein farbloses Natriumsalz des Anions Triphosphat, gehört zu den Phosphaten und hat die Summenformel Na5P3O10. Der Name Triphosphat wird gelegentlich anstelle von Pentanatriumtriphosphat verwendet. Triphosphate sind auch Teile wichtiger organischer Verbindungen wie z. B. des Adenosintriphosphats. Es ist in der EU als Lebensmittelzusatzstoff der Nummer E 451 zugelassen.
Inhaltsverzeichnis
Synthese
Pentanatriumtriphosphat entsteht durch Kondensation der ortho-Phosphorsäure:
Im Labor erhält man es aus Natriumphosphat und Natriumdiphosphat:
Möglich ist auch die Herstellung aus Natriumtrimetaphosphat:[3]
Eigenschaften
Pentanatriumtriphosphat ist ein hygroskopischer, weisser, geruchloser, nicht brennbarer Feststoff, welcher leicht löslich in Wasser ist. Er zersetzt sich ab einer Temperatur von 622 °C, wobei Phosphoroxide und Natriumoxid entstehen. Seine wässrige Lösung reagiert alkalisch.[2]
Verwendung
Triphosphate werden in Waschmitteln verwendet, um das Wasser zu enthärten und somit die Tenside in ihrer Wirkung zu unterstützen. Die Triphosphatanionen des Pentanatriumtriphosphats zum Beispiel bilden mit Calcium- und Magnesiumionen stabile und wasserlösliche Verbindungen. Es handelt sich also um einen guten Komplexbildner, der verhindert, dass sich schwer lösliche Verbindungen, so genannte „Kalkseifen“, aus den Erdalkalimetallen bilden, die sich dann beispielsweise an den Heizstäben in Waschmaschinen oder auf der Wäsche absetzen und somit die Wirkung des Waschmittels, der Tenside, behindern.
Moderne Kläranlagen halten den größten Teil der im Abwasser enthaltenen und als Nährstoff von Mikroorganismen und Pflanzen benötigten Phosphate zurück. Dennoch wird ein großer Teil der Waschmittel-Phosphate heutzutage durch Zeolith A – ein Natriumaluminiumsilicat – ersetzt, um eine Überdüngung der Oberflächengewässer durch Phosphate zu verhindern.
Einzelnachweise
- ↑ a b c d e Datenblatt Pentanatriumtriphosphat bei Merck, abgerufen am 19. Januar 2011.
- ↑ a b c Eintrag zu CAS-Nr. 7758-29-4 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 29. Mai 2011 (JavaScript erforderlich).
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 547–8.
Kategorien:- Antioxidationsmittel
- Lebensmittelkonservierungsstoff
- Natriumverbindung
- Phosphat
Wikimedia Foundation.




