- Selenwasserstoff
-
Strukturformel 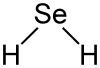
Allgemeines Name Selenwasserstoff Andere Namen - Hydrogenselenid
- Dihydrogenselenid
- Selan
Summenformel H2Se CAS-Nummer 7783-07-5 PubChem 533 Kurzbeschreibung farbloses Gas mit stechendem Geruch[1]
Eigenschaften Molare Masse 80,98 g·mol−1 Aggregatzustand gasförmig
Dichte Schmelzpunkt Siedepunkt −41 °C (Zersetzung oberhalb von 150 °C)[2]
Dampfdruck Löslichkeit schlecht in Wasser (9,8 g·l−1)[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar H- und P-Sätze H: siehe oben EUH: siehe oben P: siehe oben EU-Gefahrstoffkennzeichnung [2] 

Hoch-
entzündlichSehr giftig (F+) (T+) R- und S-Sätze R: 12-26 S: (1)-9-16-33-36-45 MAK 0,015 ml·m−3[2]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Selenwasserstoff, auch Monoselan, ist eine Verbindung aus Selen und Wasserstoff. Sie entsteht beim Auflösen salzartiger Selenide in verdünnten Säuren. Selenwasserstoff ist ein farbloses, äußerst giftiges Gas mit unangenehm fauligem Geruch. Bereits einmaliges Einatmen kleiner Mengen führt zu unangenehmen, lange anhaltenden Reizungen der Schleimhäute (sog. „Selenschnupfen“). Selenwasserstoff ist giftiger als Schwefelwasserstoff. Bei Laborversuchen, bei denen auch nur sehr geringe Mengen Selenwasserstoff entstehen, muss unbedingt unter einem Abzug gearbeitet werden und ein gasdichter Schutzanzug getragen werden.
Selenwasserstoff dient in der Halbleiter- und Elektronikindustrie zur Dotierung von Halbleitern.
Inhaltsverzeichnis
Physikalische Eigenschaften
Selenwasserstoff ist gewinkelt gebaut (Bindungswinkel 91°), die Bindungslänge Se–H beträgt 146 pm.[4]
Weitere Eigenschaften Eigenschaft Wert Kritische Temperatur 138 °C[1] Kritischer Druck 8,92 MPa[1] Kritische Dichte 0,76 kg/l Tripelpunkt Temperatur −65,65 °C Tripelpunkt Druck 0,2738 bar Herstellung
Zu reinem Selenwasserstoff führt im Labor das Auflösen von trockenem Aluminiumselenid in Wasser, oder eine Reaktion der Elemente bei 400 °C:[5]
Weblinks
Einzelnachweise
- ↑ a b c Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d e f g h Eintrag zu CAS-Nr. 7783-07-5 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30.08.2007 (JavaScript erforderlich).
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Nils Wiberg, Egon Wiberg, Arnold Fr. Holleman: Lehrbuch der Anorganischen Chemie. 102., stark umgearb. u. verb. Auflage, Gruyter Verlag, 2007, ISBN 978-3-11-017770-1, S. 627.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., Band 1, Academic Press 1963, S. 418-9.
Wikimedia Foundation.



