- Steroid-5α-Reduktase
-
Steroid-5α-Reduktase 1 —
Masse/Länge Primärstruktur 259 Aminosäuren; 29,5 kDa Bezeichner Gen-Namen SRD5A1; S5AR Externe IDs OMIM: 184753 MGI: 98400 Enzymklassifikation EC, Kategorie 1.3.99.5 Oxidoreduktase Reaktionsart Hydrierung Substrat 3-Oxo-Δ4,5-Steroid Produkte 3-Oxo-5α-Steroid Vorkommen Übergeordnetes Taxon Euteleostomi Orthologe Mensch Maus Entrez 6715 78925 Ensembl ENSG00000145545; ENSMUSG00000021594 UniProt P18405 Q68FF9 Refseq (mRNA) NM_001047 NM_175283 Refseq (Protein) NP_001038 NP_780492 Genlocus Chr 5: 6.69 - 6.72 Mb Chr 13: 69.71 - 69.75 Mb PubMed Suche [1] [2] Steroid-5α-Reduktase 2 —
Masse/Länge Primärstruktur 254 Aminosäuren; 28,4 kDa Bezeichner Gen-Name SRD5A2 Externe IDs OMIM: 607306 MGI: 2150380 Enzymklassifikation EC, Kategorie 1.3.99.5 Oxidoreduktase Reaktionsart Hydrierung Substrat 3-Oxo-Δ4,5-Steroid Produkte 3-Oxo-5α-Steroid Vorkommen Übergeordnetes Taxon Euteleostomi Orthologe Mensch Maus Entrez 6716 94224 Ensembl ENSG00000049319 ENSMUSG00000038541 UniProt P31213 Q99N99 Refseq (mRNA) NM_000348 NM_053188 Refseq (Protein) NP_000339 NP_444418 Genlocus Chr 2: 31.6 - 31.66 Mb Chr 17: 74.37 - 74.4 Mb PubMed Suche [3] [4] Steroid-5α-Reduktase (SRD5) ist der Name für zwei Enzyme, die in Wirbeltieren vorkommen und sehr ähnlich sind (sogenannte Isozyme). Beide Isozyme ermöglichen die Umwandlung des Sexualhormons Testosteron in das biologisch wirksamere Dihydrotestosteron und sind damit für die Wirkungen dieses Hormons notwendig. Das Fehlen insbesondere des zweiten Isozyms (SRD5A2) führt bei Männern zur Fehlbildung der Harnröhre, der sogenannten Hypospadie, und bei Frauen zu erhöhtem Risiko für polyzystisches Ovarialsyndrom. Andererseits hat die Hemmung der Enzyme günstige Wirkungen bei Krankheiten der Prostata und bei Haarausfall.
Inhaltsverzeichnis
Struktur
Vom Enzym existieren zwei Isoformen, die als 5α-Reduktase Typ I[1] und 5α-Reduktase Typ II[2] bezeichnet werden und deren Gene (SRD5A1 und SRD5A2) auf verschiedenen Chromosomen (5 und 2) liegen. Die Primärstruktur der beiden hydrophoben Membranproteine besteht aus 259 bzw. 254 Aminosäuren, mit einer Molekülmasse von 29.459 Da respektive 28.393 Da.
Biologische Funktion
-
Metabolismus der Steroidhormone
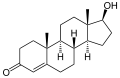
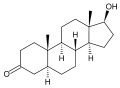
Steroid-5α-Reduktase ist ein NADPH-abhängiges Enzym aus der Gruppe der Oxidoreduktasen, welches irreversibel die Reduktion von 3-Oxo-Δ4,5-Steroiden zu den korrespondierenden 3-Oxo-5α-Verbindungen katalysiert. Die mit Abstand wichtigste Reaktion ist dabei die Umwandlung des Sexualhormons Testosteron in das biologisch wirksamere Dihydrotestosteron (DHT).[3]
Physiologie
Die beiden Isoenzyme werden nicht nur in bestimmten Organen beziehungsweise Gewebe des männlichen menschlichen Körpers produziert. Dies sind insbesondere die Haut, die Samenblase, die Prostata und die Nebenhoden. Erhöhte Produktion des Enzyms findet auch in polyzystischen Ovarien der Frau statt, weshalb es möglicherweise eine Rolle beim polyzystischen Ovarialsyndrom spielt.[4]
Der Mangel oder gar die Abwesenheit vom Typ 2 im männlichen Fötus kann zur Hypospadie und Intersexualität führen.[5]
Eine Inhibierung der beiden Isoenzyme der 5α-Reduktase führt zu einer verminderten Produktion von Dihydrotestosteron und zu einem erhöhtem Spiegel an Testosteron, zum Teil auch von Estradiol. Die Ausbildung einer Gynäkomastie und ist dabei nur eine der möglichen Nebenwirkungen der 5α-Reduktase-Inhibierung.[4]
Pharmakologie
5α-Reduktase-Inhibitoren sind Arzneimittel, die beispielsweise in der Therapie der benignen Prostatahyperplasie (BPH), Prostatakrebs, Pubertas praecox, Hirsutismus oder auch bei Alopezie Verwendung finden. Beispiele hierfür sind Finasterid und Dutasterid. Finasterid blockiert nur die Funktion des Isoenzymes (Typ 2), während Dutasterid beide Typen inhibiert.
Diese Inhibitoren leiten sich von der Struktur des Testosteron ab. Es ist bisher noch nicht gelungen, die Strukturen der Isoenzyme mittels Röntgenstrukturanalyse näher zu untersuchen. Die einzig verfügbare Information ist die von der cDNA abgeleitete Primärstruktur der Proteine.[3]
Einzelnachweise
- ↑ UniProt P18405.
- ↑ UniProt P31213.
- ↑ a b Streiber, M. (2006): Hybridinhibitoren der humanen 5α-Reduktase: Ein neues Konzept zur Hemmung der 5α-Reduktase Isoenzyme Typ I und Typ II. Dissertation, Universität Saarbrücken. PDF
- ↑ a b SRD5AR2 bei Online Mendelian Inheritance in Man.
- ↑ Pseudovaginal Perineoscrotal Hypospadia bei Online Mendelian Inheritance in Man.
Literatur
- Andersson S et.al., Deletion of steroid 5 alpha-reductase 2 gene in male pseudohermaphroditism., in Nature, 354/1991, S. 159–161.
- Imperato-McGinley J et.al., Steroid 5alpha-reductase deficiency in man: an inherited form of male pseudohermaphroditism., in Science, 186/1974, S. 1213–1215.
- Andersson S et.al., Structural and biochemical properties of cloned and expressed human and rat steroid 5 alpha-reductases., in Proc Natl Acad Sci, 87/1990, S. 3640–3644.
- Russell DW et.al., Steroid 5 alpha-reductase: two genes/two enzymes., in Annu Rev Biochem, 63/1994, S. 25–61.
- Ishikawa T et.al., Aromatase-independent testosterone conversion into estrogenic steroids is inhibited by a 5 alpha-reductase inhibitor., in J Steroid Biochem Mol Biol., 98/2006, S. 133–138.
- Iranmanesh A et.al., Combined inhibition of types I and II 5 alpha-reductase selectively augments the basal (nonpulsatile) mode of testosterone secretion in young men, in J Clin Endocrinol Metab, 90/2005, S. 4232–4237.
- Choi MH et.al., Biochemical roles of testosterone and epitestosterone to 5 alpha-reductase as indicators of male-pattern baldness., in J Invest Dermatol. 116/2001, S. 57–61.
Weblinks

Bitte den Hinweis zu Gesundheitsthemen beachten!
Wikimedia Foundation.