- Barbaloin
-
Strukturformel 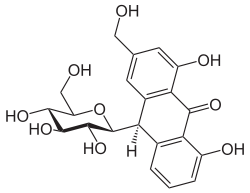
Allgemeines Name Barbaloin Andere Namen - Aloin-A
- 10-(1',5'-Anhydroglucosyl)aloe-emodin-9-anthron
- 1,8-Dihydroxy-3-hydroxymethyl- 10-(β)-D-(glucopyranosyl)anthron
Summenformel C21H22O9 CAS-Nummer 1415-73-2 Eigenschaften Molare Masse 418,4 g·mol−1 Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Achtung
H- und P-Sätze H: 315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [1] EU-Gefahrstoffkennzeichnung [1] 
Reizend (Xi) R- und S-Sätze R: 36/37/38 S: 26-36 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Barbaloin (auch Aloin-A) gehört zur Gruppe der Anthracenderivate, genauer betrachtet ist es ein Anthrachinonglycosid. Es kristallisiert in gelben Nadeln, riecht schwach nach Aloe und hat einen bitteren Geschmack. Aloin-A (Barbaloin) kommt neben dem diastereomeren Aloin-B in unterschiedlichen Verhältnissen in Aloen vor, was vorwiegend von der jeweiligen Spezies abhängt. Treten beide Stoffe als Gemisch auf, so spricht man meist allgemein vom Aloin, Meist überwiegt der Anteil von Aloin-A. Dem früher als Isobarbaloin bezeichneten und durch die Rosenthaler-Reaktion identifizierten Inhaltsstoff konnte 1982 von Vötig die Struktur des 7-Hydroxyloin zugeordnet werden, das ebenfalls in beiden diastereomeren Formen aus der westindischen Aloe isoliert werden konnte. Es kommt nicht in der Kapaloe vor.[2]
Inhaltsverzeichnis
Geschichte
1851 wurde Aloin erstmals als Naturstoff aus Barbados-Aloe isoliert. Dieses wurde von E. Leger 1897 als Anthrachinon-Derivat erkannt. Erst 1952 gelang es Mühlemann, die korrekte Struktur zu ermitteln.
Vorkommen
Zurzeit ist bekannt, dass Aloin nicht nur in über 20 Aloe-Arten, sondern auch in amerikanischer Faulbaumrinde (Rhamnus purshiana, Rhamnaceae) vorkommt. Der Gehalt an Aloin in verschiedenen Aloe-Sorten schwankt je nach ihrer Art, Herkunft und Saisonbedingungen in den Grenzen von 5 bis 40 % (bezogen auf die Aloe-Droge). In-vivo-Untersuchungen zur Biosynthese der Aloine haben gezeigt, dass Aloin-B von der Pflanze aktiv synthetisiert wird, während das Isomer Aloin-A sekundär durch Umwandlung aus Aloin-B entsteht.
Gewinnung und Darstellung
Neben der Extraktion aus getrockneter Aloe und anschließender Aufarbeitung mittels Umkristallisation oder Säulenchromatographie, gelingt es auf nasschemischen Weg aus Aloeemodin-9-anthron, α-Bromacetoglucose und Natriumhydroxid das Diasteromerengemisch aus Aloin-A und Aloin-B zu synthetisieren.
Verwendung
Aloin-A findet in der Medizin wie auch Naturheilkunde Verwendung als Laxans (Laxativum) zur Darmentleerung. Dabei stellt das Aloin-A als Anthrachinonglycosid nur die Transportform dar, welche durch bakterielle Enzyme in die Wirkfom überführt wird. Weiterhin kann es in der Chemie als Ausgangsstoff für strukturelle Veränderungen eingesetzt werden. Es wurde von weiteren Verwendungen bei Hepatitis B und Herpes berichtet.
Aloins wird als Bitterstoff Getränken beigemischt. Nach deutschen Recht gemäß der Aromenordnung ist der Gehalt wie folgt festgelegt:
- Getränke – 0,1 mg/kg
- andere Lebensmittel – 0,1 mg/kg
- alkoholischen Getränke – 50 mg/kg
In kosmetischen Mitteln ist für Aloin keine maximale Gebrauchskonzentration festgelegt.
Sicherheitshinweise
Aloin kann bei häufiger Anwendung als Laxans die Oberfläche des Dünndarmes schädigen und einen Elektrolytmangel hervorrufen. Weiterhin kann es zu genotoxischen und tumorpromovierenden Wirkungen kommen.
Nachweis
Eine vorher in Chloroform aufgenommene Probe zeigt – auf ein Probemedium (TLC-Platte) aufgetragen – nach dem Besprühen mit einer methanolischen 10 % KOH-Lösung eine gelbe Farbe die sich unter UV-Licht (365 nm) verstärkt. Dieser Nachweis beruht auf der Tatsache, das sich im Alkalischen das Anthron-Anthranol-Gleichgewicht auf die Seite der Anthranolform verschiebt. Mittels UV-VIS-Spektroskopie kann man drei Maxima bei 297, 287 und 354 nm beobachten.
Einzelnachweise
Kategorien:- Reizender Stoff
- Polyphenol
- Keton
- Benzylalkohol
- Glycosid
Wikimedia Foundation.
