- Vildagliptin
-
Strukturformel 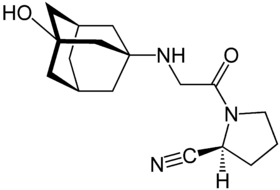
Allgemeines Freiname Vildagliptin Andere Namen (2S)-{((3-Hydroxyadamantan-1-yl)amino) acetyl}pyrrolidin-2-carbonitril (IUPAC)
Summenformel C17H25N3O2 CAS-Nummer 274901-16-5 PubChem 6918537 ATC-Code A10BH02
Arzneistoffangaben Wirkstoffklasse Wirkmechanismus Verschreibungspflichtig: ja Eigenschaften Molare Masse 303,40 g·mol−1 Schmelzpunkt Löslichkeit sehr gut in Wasser und organischen Lösungsmitteln
Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln EU-Gefahrstoffkennzeichnung [2] Keine Einstufung verfügbarR- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Vildagliptin ist ein orales Antidiabetikum, das im Frühjahr 2008 von Novartis in den Markt eingeführt wurde. Der Wirkstoff wurde europaweit durch die Europäische Arzneimittelagentur zugelassen.[3] Das Adamantanderivat Vildagliptin ist nach Sitagliptin der zweite Arzneistoff aus der neuen Klasse der Dipeptidyl-Peptidase-4-Inhibitoren und wurde nach seinem Entdecker, dem Chemiker Edwin B. Villhauer, benannt. Anders als die Inkretinmimetika wie Exenatid ahmen diese Gliptine nicht die Struktur der Inkretine nach, sondern behindern deren Abbau. Wie alle neu zugelassenen Arzneistoffe ist auch Vildagliptin verschreibungspflichtig.
Inhaltsverzeichnis
Wirkungsweise und Pharmakologie
Inkretine
Das glukoseabhängige insulinotrope Peptid (GIP) und das Glucagon-like Peptid 1 (GLP-1) sind Inkretine, die vom Darm fortwährend in die Blutbahn sezerniert werden. Die Inkretin-Abgabe wird nach einer Mahlzeit gesteigert. Sowohl GIP als auch GLP-1 erhöhen die Synthese und die Freisetzung des Insulins aus den β-Zellen der Langerhans-Inseln, die sich wiederum im Pankreas befinden. GLP-1 senkt außerdem die Glucagon-Exkretion, dessen Hauptaufgabe die Blutzuckerspiegel-Erhöhung ist und das in den α-Zellen gebildet und gespeichert wird. Die Inkretine wirken nur auf die Insulin-Freisetzung, wenn der Glucose-Blutspiegel nach einer Nahrungsaufnahme hoch ist. Ein Vorteil dieser Wirkweise ist, dass eine Hypoglykämie (also eine zu starke Blutzuckerspiegel-Absenkung mit Folgen bis zu Krämpfen und Bewusstlosigkeit) durch die Einnahme dieses Wirkstoffs nicht eintreten kann, was bei einigen anderen Antidiabetika möglich ist. Auch die Glucagon-Freisetzungshemmung findet nur bei erhöhtem Glucose-Blutspiegel statt.
Funktion der Dipeptidyl-Peptidase-4
- siehe auch Hauptartikel: Dipeptidyl-Peptidase-4
Die Dipeptidyl-Peptidase-4 (DPP4) ist eine Exopeptidase, sie spaltet von Proteinen (am N-terminalen Ende) ein Dipeptid ab. Das aus dem Darm freigesetzte GLP-1 wird so innerhalb von wenigen Minuten inaktiviert und trägt nicht mehr zur Blutglucosespiegel-Senkung bei.
Hemmwirkung des Vildagliptins
Vildagliptin ist ein Substrat von DPP4, anders als Sitagliptin, das ein kompetitiver Inhibitor der DPP4 ist. Es hemmt das Enzym DPP4 etwa zwei Stunden lang, was die Wirkzeit von Vildagliptin gegenüber Sitagliptin steigert. Vildagliptin steigert also durch seine DPP4-Hemmung den Blutspiegel von GLP-1 und sorgt für ein längeres Verbleiben von GLP-1 im Blut, weil GLP-1 weniger rasch abgebaut werden kann. Durch die gesteigerte und zeitlich verlängerte Anwesenheit des GLP-1 wird die Insulin-Produktion und -Ausschüttung gesteigert und die Glucagonabgabe gebremst. Durch all diese Effekte wird der Blutglucosespiegel gesenkt. Ebenso wurde die Absenkung des HbA1c-Werts nachgewiesen, was die dauerhafte Blutzuckerspiegel-Senkung über die letzten 8 Wochen vor der HbA1c-Wert-Messung widerspiegelt.
Darreichungsform
Vildagliptin wird durch den Patienten peroral aufgenommen, unzerkaut und mit etwas Wasser. Die Monopräparat-Tablette mit 50 mg Vildagliptin ist (laut den Zulassungsunterlagen) eine hellgelbliche Tablette, die flach und rund ist und einen Durchmesser von 8 mm hat. Die Monopräparat-Tablette, die 100 mg Vildagliptin enthält, ist weiß bis hellgelblich und länglich (14 x 5,5 mm). Die Kombinationspräparat-Tablette ist eine gelbe Filmtablette von ovaler Form mit einer abgeschrägten Kante.
Anwendungsgebiete
Vildagliptin wird in einer Zweifachkombination zur Behandlung des Diabetes mellitus Typ 2 angewendet und wird kombiniert entweder mit Metformin, einem Sulfonylharnstoff oder einem Thiazolidindion, wenn die jeweilige Einzelsubstanz-Therapie nicht ausreicht, um den Blutzucker ausreichend einzustellen. Die Unbedenklichkeit und Wirksamkeit von Vildagliptin in einer Dreifachkombination sind dagegen nicht nachgewiesen. Auch der HbA1c-Wert sinkt durch Therapie mit Vildagliptin. Die empfohlene Tagesdosis beträgt je nach Komedikation entweder 50 mg oder 100 mg und soll auf zwei Tagesgaben (je 50 mg) aufgeteilt werden. Vildagliptin kann mit oder ohne Nahrung eingenommen werden.[4]
Gegenanzeigen
absolute Kontraindikationen
Vildagliptin darf nicht angewendet werden:
- beim Vorliegen eines Diabetes mellitus Typ 1
- zur Behandlung einer Ketoazidose
- beim Bestehen schwerer Leberfunktionsstörungen, da es Transaminasen (Leberwerte) erhöhen kann
- beim Bestehen einer Schwangerschaft
relative Kontraindikationen
nicht empfohlen wird die Anwendung von Vildagliptin:
- bei Patienten mit mittelschweren bis starken Nierenfunktionsstörungen und bei Dialyse-Patienten mit Terminaler Niereninsuffuzienz wegen begrenzter Erfahrung
- bei Patienten mit Herzinsuffizienz der Stufen NYHA III-IV wegen mangelnder Erfahrung
Interaktionen
Wechselwirkungen mit anderen Arzneimitteln wurden in den klinischen Studien nicht beobachtet. Die Wahrscheinlichkeit für Wechselwirkungen ist deshalb so gering, weil Vildagliptin nicht über die Cytochrom P450-Superfamilie metabolisiert wird und somit weder den Abbau von Cytochrom-P450-metabolisierten Wirkstoffen behindern noch in ihrem Abbau behindert werden und auch kein Cytochrom-P450-Isoenzym induzieren. Möglicherweise kann, analog zu Interaktionen bei anderen Antidiabetika, die Blutglucosespiegel-Senkung durch Thiazid-Diuretika, Corticosteroide, Schilddrüsenarzneimittel und Sympathomimetika beeinträchtigt sein.
Nebenwirkungen
Bei einer Monotherapie mit Vildagliptin kam es gelegentlich (mindestens bei jedem tausendsten Probanden und maximal bei jedem hundertsten) zu einer Hypoglykämie und Anstieg der Transaminasen (Leberenzyme). Ein solcher Leberenzymanstieg ist Hinweis auf mögliche Leberschäden. Die Leberwerte sind unter Therapie zu kontrollieren. Aufgrund möglicher Leberschäden darf das Medikament nicht wie geplant einmal täglich genommen werden, sondern muss auf zwei Tagesdosen aufgeteilt werden. Auffallend sind Harnwegsinfekte, die in einer Studie fast dreimal häufiger als unter Placebo auftraten.
In Kombination mit Metformin kam es häufig (mindestens bei jedem hundertsten Probanden und maximal bei jedem zehnten) zu Tremor, Kopfschmerzen, Schwindel, Hypoglykämie (etwas häufiger als bei Metformin + Placebo), Übelkeit und gelegentlich zu Müdigkeit.
In Kombination mit einem Sulfonylharnstoff kam es häufig zur Hypoglykämie (bei Vildagliptin und Glimepirid etwas häufiger als bei Placebo und Glimepirid), Tremor, Kopfschmerzen, Schwindel, Asthenie sowie gelegentlich zu Verstopfung. Sehr selten (weniger als bei jedem zehntausendstem Probanden) trat eine Nasopharyngitis (Entzündung der Nasen- und Rachen-Schleimhaut).
In Kombination mit einem Thiazolidindion wurde häufig ein Anstieg des Körpergewichts und periphere Ödeme beobachtet, gelegentlich Kopfschmerzen und Asthenie.
Nutzen-/Risikobetrachtung
Vildagliptin senkt den HbA1c (ein Surrogatmarker für die Blutzuckereinstellung) 0,5% bis 0,8% (50 mg) bzw. 0,7% bis 1,1% (100 mg) gegenüber Placebo. Dies ist etwas schlechter als andere orale Antidiabetika. Gegenüber Rosiglitazon und Metformin konnte keine Nicht-Unterlegenheit nachgewiesen werden. Es liegen keine Daten zur Langzeitsicherheit oder zur Wirkung auf Spätkomplikationen des Diabetes mellitus vor.
Pharmakokinetik
Resorption
Wird die Tablette mit dem Wirkstoff nüchtern eingenommen, so werden nach 1,7 Stunden die maximalen Plasmaspiegel erreicht. Sofern die Tablette nach einer Mahlzeit eingenommen wurde, verschiebt sich das dann etwas niedrigere Plasmaspiegel-Maximum auf etwa 2,5 Stunden nach der Aufnahme. In beiden Fällen betrug die Bioverfügbarkeit 85 %.
Verteilung
Vildagliptin hat eine Plasmaproteinbindung von 9,3%, was die Gefahr von Arzneistoff-Wechselwirkungen durch Plasmaprotein-Verdrängung nahezu ausschließt. Das Verteilungsvolumen im Steady state nach i.v.-Verabreichung beträgt 71 Liter, was darauf hindeutet, dass sich Vildagliptin nicht nur im Blutkreislauf verteilt.
Metabolisierung
69 % der Vildagliptin-Gesamtdosis werden verstoffwechselt. 57 % der Gesamtdosis werden an der Cyano-Gruppe hydrolysiert, wobei der inaktive Carbonsäure-Metabolit entsteht. 4 % der Gesamtdosis werden an der Amidbindung hydrolysiert. Auch DPP4 trägt teilweise zur Hydrolysierung von Vildagliptin bei. Über Isoenzyme der Cytochrom-P450-Superfamilie wird Vildagliptin (laut in-vitro-Untersuchungen) nicht metabolisiert.
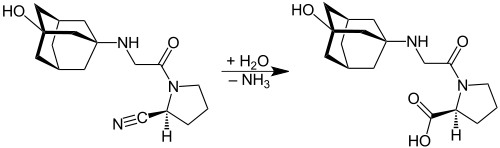 Nitril-Hydrolyse: Hydrolyse von Vildagliptin an der Nitril-Gruppe (Cyano-Gruppe). Die Nitril-Gruppe (-C≡N) wird zur Carbonsäure (-COOH) und Ammoniak wird abgespalten. 57 % der Gesamtdosis an Vildagliptin wird auf diesem Weg abgebaut.
Nitril-Hydrolyse: Hydrolyse von Vildagliptin an der Nitril-Gruppe (Cyano-Gruppe). Die Nitril-Gruppe (-C≡N) wird zur Carbonsäure (-COOH) und Ammoniak wird abgespalten. 57 % der Gesamtdosis an Vildagliptin wird auf diesem Weg abgebaut.
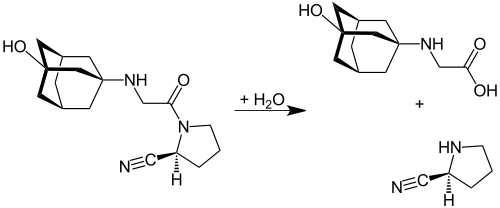 Amid-Hydrolyse: Hydrolyse von Vildagliptin an der Amid-Bindung . 4 % der Gesamtdosis an Vildagliptin wird entsprechend dieser Reaktion metabolisiert.
Amid-Hydrolyse: Hydrolyse von Vildagliptin an der Amid-Bindung . 4 % der Gesamtdosis an Vildagliptin wird entsprechend dieser Reaktion metabolisiert.
Elimination
Etwa 85 % der Gesamtdosis werden über den Urin ausgeschieden, 15 % über den Fäzes. Die Eliminationshalbwertszeit beträgt nach intravenöser Verabreichung etwa 2 Stunden und 3 Stunden nach der zur Therapie vorgesehenen peroralen Einnahme.
Chemie
Der Name von Vildagliptin nach der IUPAC-Nomenklatur ist (2S)-{((3-Hydroxyadamantan-1-yl)amino)acetyl}pyrrolidin-2-carbonitril; es ist damit ein Derivat des Adamantan. Vildagliptin ist ein weißes bis leicht gelbliches oder leicht graues kristallines Pulver, polymorphe Modifikationen sind bislang unbekannt. Es ist nicht hygroskopisch und sehr gut löslich in Wasser und organischen Lösungsmitteln. Vildagliptin hat ein Chiralitätszentrum und somit zwei Enantiomere, von denen das (S)-Enantiomer (das Eutomer) als Arzneistoff eingesetzt wird. Das (R)-Enantiomer ist das biologisch unwirksame Distomer.
Handelsnamen
Galvus (D, A, CH), Jalra (A), Xiliarx (A)
Eucreas (D, A), Zomarist (A)
Einzelnachweise
- ↑ The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1716, ISBN 978-0-911910-00-1.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ EPAR der Europäischen Arzneimittelagentur.
- ↑ Pharmazeutische Zeitung Nr. 44/2007, S. 26 ff.
Weblinks
- European Public Assessment Report (EPAR) der Europäischen Arzneimittelagentur für Galvus®
- European Public Assessment Report (EPAR) der Europäischen Arzneimittelagentur für Eucreas®

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-A10
- Nitril
- Carbonsäureamid
- Alpha-Aminocarbonyl
- Alkohol
- Pyrrolidin
- Cyclohexan
- Arzneistoff
- Antidiabetikum
- Enzyminhibitor
Wikimedia Foundation.
