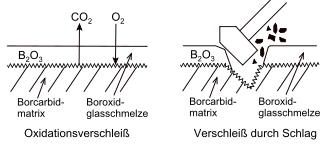- Borcarbid
-
Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Borcarbid Andere Namen Schwarzer Diamant
Verhältnisformel B4C CAS-Nummer 12069-32-8 Kurzbeschreibung glänzende schwarze Kristalle oder schwarzes Pulver[1]
Eigenschaften Molare Masse 55,25 g·mol−1 Aggregatzustand fest
Dichte 2,51 g·cm−3[2]
Schmelzpunkt Siedepunkt >3500 °C[1]
Löslichkeit unlöslich in Wasser[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 332 EUH: keine EUH-Sätze P: keine P-Sätze [3] EU-Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 20-36/37/38 S: 9-26-36/37 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Borcarbid (Summenformel B4C) ist ein sehr hartes Material mit einer Mohshärte von 9,3, welches als verschleißbeständiges Material genutzt wird. Borcarbid wird häufig als Metallcarbid klassifiziert; dies ist sehr umstritten, da Bor kein Metall ist. Die Differenz der Elektronegativität zwischen Bor und Kohlenstoff ist deutlich kleiner als 1,5; somit sind im Unterschied zu den metallischen (Einlagerungs-)Carbiden wie zum Beispiel Titancarbid (TiC) kovalente Nichtmetall-Nichtmetall-Bindungen vorhanden.
Inhaltsverzeichnis
Gewinnung und Darstellung
Je nach Herstellungsverfahren erhält man Borcarbid als feines schwarzes Pulver oder in Gestalt grober schwarzglänzender Kristalle.
Das grobkristalline Borcarbid fällt bei der Herstellung aus Bortrioxid und Kohlenstoff im elektrischen Widerstandsofen bei 2400 °C an:

- Herstellung von grobkristallinem Borcarbid
Das feinkristalline Pulver entsteht bei der Reduktion von Bortrioxid mit Magnesium in Gegenwart von Kohlenstoff:
- Herstellung von pulverförmigem Borcarbid
Eigenschaften
Physikalische Eigenschaften
Borcarbid ist eine Nichtoxid-Keramik, die sich ähnlich wie Siliciumcarbid oder Siliciumnitrid durch besondere Härte und Zähigkeit auszeichnet. Borcarbid-Keramik ist sehr verschleißbeständig bei niedrigen Temperaturen. Sie sind in Hinsicht auf ihre Härte sogar verschleißbeständiger als Siliciumnitrid-Keramiken, jedoch nur bei niedrigen Temperaturen, siehe unten.
Borcarbid ist ein effektiver Neutronenabsorber und wurde z.B. bei der Katastrophe von Tschernobyl in den explodierten Reaktor abgeworfen, um die Kettenreaktion einzudämmen.
Verschleißmechanismus
Borcarbid verschleißt ebenso wie andere Werkstoffe mechanisch, indem durch Krafteinwirkung (Schlag, Reibung) Teile des Gefüges herausgebrochen werden. Da aber Borcarbid ein sehr harter Werkstoff ist, sogar der härteste, der wirtschaftlich synthetisiert werden kann, unterliegt er diesem Verschleiß nur in geringem Maße. Ähnlich harte und verschleißbeständige Materialien sind Siliciumnitrid oder Siliciumcarbid.
Borcarbid widersteht der Oxidation durch Passivierung, indem die Oberfläche des Materials mit Sauerstoff reagiert:
 bzw.
bzw.
Bei der Reaktion ist die Temperatur wesentlich, in Folge des Boudouard-Gleichgewichtes kann je nachdem Kohlenstoffmonoxid oder Kohlenstoffdioxid entstehen. Das gebildete Bortrioxid ist ein Festkörper, der in kristalliner Form bei 450 °C schmilzt, in amorpher oder glasiger schon bei niedrigerer Temperatur. Seine Schmelze hindert den Sauerstoffzutritt in die Borcarbid-Matrix, so dass deren weitere Oxidation behindert wird. Leider werden bei Verschleißanwendungen häufig Temperaturen deutlich über 450 °C erreicht, bei denen Bortrioxid dann schon recht dünnflüssig ist. Dann kann Luftsauerstoff leichter durch die Bortrioxidschmelze diffundieren. Bei der Oxidation der konkurrierenden Werkstoffe Siliciumnitrid und Siliciumcarbid entsteht dagegen Siliciumdioxid, das wesentlich zähflüssiger ist als Bortrioxid und durch dessen Schmelze der Luftsauerstoff deshalb weniger diffundiert. Siliciumnitrid oder Siliciumcarbid widerstehen deshalb der Oxidation besser.
Chemische Eigenschaften
Borcarbid ist ein chemisch sehr inertes Material. Es wird erst oberhalb von 1000 °C von Chlor oder Sauerstoff merklich angegriffen. Gegen Fluorwasserstoff und heiße Salpetersäure ist es vollkommen beständig.
Verwendung
- Panzerungsmaterial
- als Schneidstoff in der Werkzeugbearbeitung
- Neutronenabsorber in Kernkraftwerken
- Werkstoff für Sandstrahldüsen
Einzelnachweise
Kategorien:- Gesundheitsschädlicher Stoff
- Werkzeugwerkstoff
- Carbid
- Nicht-Oxidkeramik
- Borverbindung
Wikimedia Foundation.