- Bromoform
-
Strukturformel 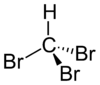
Allgemeines Name Bromoform Andere Namen - Tribrommethan
- Methenyltribromid
Summenformel CHBr3 CAS-Nummer 75-25-2 Kurzbeschreibung farblose chloroformähnlich riechende Flüssigkeit[1]
Eigenschaften Molare Masse 252,75 g·mol−1 Aggregatzustand flüssig
Dichte 2,8899 g·cm−3 (20 °C)[2]
Schmelzpunkt Siedepunkt 149,5 °C[2]
Löslichkeit - schlecht in Wasser (3,2 g·l−1 bei 30 °C)[2]
- gut in Ethanol und Diethylether[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 

Gefahr
H- und P-Sätze H: 331-302-319-315-411 EUH: keine EUH-Sätze P: 273-304+340-305+351+338-302+352-309-310 [2] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 22-23-36/38-51/53 S: (1/2)-28-45-63-61 LD50 1147 mg·kg−1 (Ratte, peroral)[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Bromoform (CHBr3) ist ein dem Chloroform ähnlicher halogenierter Kohlenwasserstoff.
Inhaltsverzeichnis
Vorkommen und Bildung
Bromoform entsteht aus Meerwasser aufgrund dessen natürlichen Bromidgehaltes. Es ist damit die stärkste Quelle organischen Broms in der Erdatmosphäre.
Es entsteht ebenfalls bei der Aufbereitung von Wasser für Kühl-, Bade- und Trinkzwecke und ist in allen chlorierten und ozonisierten Wässern enthalten. Küstenkraftwerke, die chloriertes Meerwasser zu Kühlzwecken verwenden, stellen die stärkste von Menschen erzeugte Quelle dar.
Im Labor kann Bromoform durch die sogenannte Haloform-Reaktion zum Beispiel aus Aceton (R = CH3) und Hypobromit hergestellt werden:
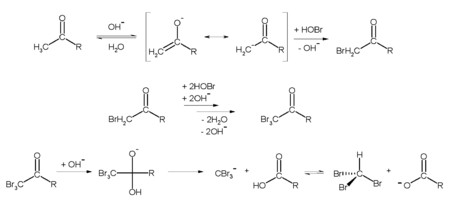
Eigenschaften
Bromoform reagiert mit vielen organischen Verbindungen, wobei giftige Bromverbindungen entstehen können. Mit Alkalimetallen reagiert es explosionsartig. Die Dämpfe sind schwerer als Luft. Beim Erhitzen über den Siedepunkt findet Selbstzersetzung statt.
Atmosphärisches Verhalten
Aus der in der Atmosphäre kurzlebigen Verbindung werden Bromradikale freigesetzt, die für fotochemische Vorgänge in der Troposphäre und Stratosphäre verantwortlich sind. Sie spielen unter anderem eine Rolle bei der Entstehung des Ozonlochs.
Einzelnachweise
- ↑ a b c Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d e f Eintrag zu Bromoform in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1.1.2008 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 75-25-2 im European chemical Substances Information System ESIS
Kategorien:- Gesundheitsschädlicher Stoff
- Umweltgefährlicher Stoff
- Giftiger Stoff
- Bromalkan
Wikimedia Foundation.
