- Dextromoramid
-
Strukturformel 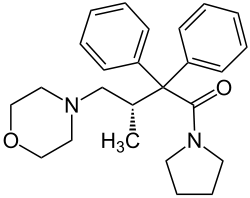
Allgemeines Freiname Dextromoramid Andere Namen (3R)-3-Methyl-4-(morpholin-4-yl)-2,2-diphenyl-1-(pyrrolidin-1-yl)butan-1-on (IUPAC)
Summenformel - C25H32N2O2
- C25H32N2O2·C4H6O6 (Bitartrat)
CAS-Nummer - 357-56-2
- 2922-44-3 (Bitartrat)
PubChem 92943 ATC-Code N02AC01
DrugBank DB01529 Arzneistoffangaben Wirkstoffklasse Verschreibungspflichtig: nicht verschreibungsfähig (D) Eigenschaften Molare Masse 392,53 g·mol−1 Schmelzpunkt Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln EU-Gefahrstoffkennzeichnung [3] Keine Einstufung verfügbarR- und S-Sätze R: siehe oben S: siehe oben LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Dextromoramid ist ein starkes synthetisches Schmerzmittel mit opiatähnlicher Wirkung. Der Arzneistoff wurde 1957 von Janssen Pharmaceutica unter dem Handelsnamen Palfium® auf den Markt gebracht.
Die Substanz ist ein Derivat des 3,3-Diphenylpropylamins und gehört zur Methadon-Gruppe. Das Molekül enthält im Unterschied zum Methadon einen Morpholin- und einen Pyrrolidin-Ring.
Inhaltsverzeichnis
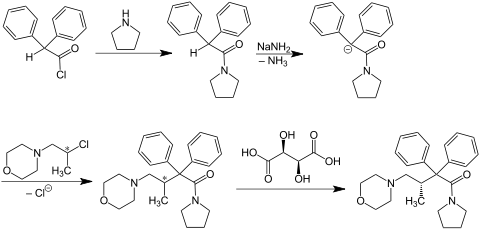
Gewinnung und Darstellung
Die Synthese von Dextromoramid geht vom Diphenylacetylchlorid aus, welches zuerst mit Pyrrolidin in das entsprechende Säureamid überführt wird. Dieses ergibt nach Umsetzung mit Natriumamid und 4-(2-Chlorpropyl)-morpholin das racemische (±)-Moramid (Racemoramid). Eine Racematspaltung mittels D-Weinsäure führt zur enantiomerenreinen Zielverbindung:[4][5]
Das bei der Racematspaltung anfallende (3S)-Enantiomer Levomoramid ist pharmakologisch inaktiv.[2][6]
Rechtliche Situation
Dextromoramid ist gemäß dem Betäubungsmittelgesetz in der Bundesrepublik Deutschland seit 1993 ein verkehrsfähiges, aber nicht verschreibungsfähiges Betäubungsmittel.[7]
Literatur
- H. J. Bochnik: Suchtentwicklung und schwere Entziehungserscheinungen nach Dextromoramidgebrauch (Jetrium, MCP 875, Palfium, R 875, Errecalme, Pyrrolamidol). In: Archives of toxicology, Bd. 18 (Nr. 3), 1960, S. 170–176.
- H. J. Roth und H. Fenner: Arzneistoffe. Thieme, Stuttgart und New York 1988, S. 336–343.
Einzelnachweise
- ↑ Thieme Römpp Online, abgerufen am 26. September 2011.
- ↑ a b Janssen, P.A.J.; Janssen, J.C.: A New Series of Potent Analgesics in J. Am. Chem. Soc. 78 (1956) 3862-3862, doi:10.1021/ja01596a087.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b c d e f A. Kleemann, J. Engel, B. Kutscher, D. Reichert: Pharmaceutical Substances – Synthesis, Patents, Applications, 4. Auflage, Thieme-Verlag, Stuttgart 2000, ISBN 978-1-58890-031-9.
- ↑ Patente BE 544 757, DE 1 117 126, GB 822 055 (Janssen 1956).
- ↑ Janssen, P.A.; Jagenau, A.M.: A New Series of Potent Analgesics: DEXTRO 2: 2-Diphenyl-3-methyl-4-morpholinobutyrylpyrrolidine and Related Amides Part I. Chemical Structure and Pharmacological Activity in J. Pharm. Pharmacol. 9 (1957) 381-400, doi:10.1111/j.2042-7158.1957.tb12290.x.
- ↑ Vierte Betäubungsmittelrechts-Änderungsverordnung – 4.BtMÄndV, vom 23. Dezember 1992.
Handelsnamen
Jetrium (D – nicht mehr im Handel), Palfium (D – nicht mehr im Handel, NL), Palface (NL)

Bitte den Hinweis zu Gesundheitsthemen beachten!
Wikimedia Foundation.