- Carbocystein
-
Strukturformel 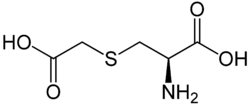
Allgemeines Freiname Carbocistein Andere Namen - S-Carboxymethyl-L-cystein
- (R)-2-Amino-4-thia-adipinsäure
- L-2-Amino-3-(carboxymethylthio) propionsäure
- 3-(Carboxymethylthio)-L-alanin
- L-3-((Carboxymethyl)thio)alanin
- L-Carboxymethylcystein
- (R)-Carbocistein
Summenformel C5H9NO4S CAS-Nummer 638-23-3 ATC-Code R05CB03
Kurzbeschreibung weißer Feststoff[1]
Arzneistoffangaben Wirkstoffklasse Verschreibungspflichtig: Ja Eigenschaften Molare Masse 179,19 g·mol−1 Aggregatzustand fest
Schmelzpunkt Löslichkeit löslich in Wasser[1]
Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln GHS-Gefahrstoffkennzeichnung [3] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze EU-Gefahrstoffkennzeichnung [1]
Xi
ReizendR- und S-Sätze R: 36/37/38 S: 26-37/39 LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Carbocystein (internationaler Freiname Carbocistein) ist ein chiraler Arzneistoff, der als Mukolytikum gegen festsitzenden Husten, wie er beispielsweise bei einer Bronchitis auftritt, eingesetzt wird.
Inhaltsverzeichnis
Wirkung und Verwendung
Carbocistein wirkt nicht durch Spaltung der Disulfidbrücken des Sekrets in den Bronchien wie Acetylcystein, sondern intrazellulär: Es wird vermehrt dünnflüssiger Schleim produziert und weniger viskoser Schleim. Seit den 1970er Jahren wird Carbocystein bei den Indikationen
- akute oder chronische Bronchitis
- Asthma- und Emphysembronchitis
- Bronchiektasen
- Bronchopneumonien
eingesetzt.
Die Wirksamkeit von Carbocystein ist umstritten, manche Experten führen die schleimlösende Wirkung auf die vermehrte Einnahme von Wasser zurück.
Eigenschaften
Der spezifische Drehwert von Carbocystein [αD20] beträgt 0,5° in 1 M Salzsäure.[4]
Chemie
Carbocystein wird aus Chloressigsäure und der natürlichen α-Aminosäure L-Cystein mithilfe von Natronlauge durch eine nucleophile Substitutionsreaktion unter Abspaltung von Natriumchlorid hergestellt[5]. Carbocistein wird ausschließlich in der enantiomerenreinen L-Form, als Arzneistoff eingesetzt. S-Carboxymethyl-L-cystein besitzt am stereogenen Zentrum (α-Kohlenstoffatom der Cystein-Substruktureinheit) (R)-Konfiguration. Die Racematspaltung von S-Carboxymethyl-DL-cystein ist in der Literatur[6] beschrieben.
Handelsnamen
Mephathiol (CH), Mucoseptal (CH), Pectorex (CH), Rhinathiol (CH), Transbronchin (D), Tussantiol (CH)
Einzelnachweise
- ↑ a b c MSDS Fischer Scientific.
- ↑ a b Carbocystein bei ChemIDplus.
- ↑ Datenblatt S-Carboxymethyl-L-cysteine bei Sigma-Aldrich, abgerufen am 27. April 2011.
- ↑ B. Staffeld: Untersuchungen zum Metabolismus von Carbocystein beim Menschen. Dissertation, FU Berlin, 1993.
- ↑ Axel Kleemann, Jürgen Engel, Bernd Kutscher und Dieter Reichert: Pharmaceutical Substances. 4. Auflage (2000), Thieme-Verlag Stuttgart, Seite 346, ISBN 978-1-58890-031-9.
- ↑ Axel Kleemann und Jürgen Martens: Optical Resolution of Racemic S-(Carboxymethyl)cysteine. In: Liebigs Annalen der Chemie 1982, S. 1995-1998.
- ↑ Rote Liste online, Stand: Oktober 2009.
- ↑ AM-Komp. d. SChweiz, Stand: Oktober 2009.

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-R05
- Reizender Stoff
- Aminosäure
- Dicarbonsäure
- Expektorans
- Antidot
- Arzneistoff
Wikimedia Foundation.
