- Vanadium(II)-iodid
-
Kristallstruktur 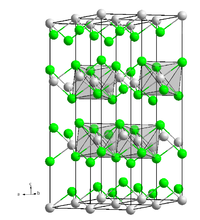
__ V2+ __ I- Allgemeines Name Vanadium(II)-iodid Andere Namen - Vanadiumdiiodid
- Vanadin(II)-iodid
- Vanadindiiodid
Verhältnisformel VI2 CAS-Nummer 15513-84-5 PubChem 84959 Kurzbeschreibung rotvioletter, kristalliner Feststoff
Eigenschaften Molare Masse 304,75 g·mol−1 Aggregatzustand fest
Dichte 5,44 g·cm−3[1]
Schmelzpunkt 750 – 800 °C[1]
Siedepunkt 850 °C[1]
Löslichkeit löst sich in Wasser unter Bildung von [V(H2O)6]2+-Ionen[2]
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Vanadium(II)-iodid ist eine chemische Verbindung der Elemente Vanadium und Iod. Es ist ein rotvioletter, kristalliner Feststoff, der bei 750 – 800 °C schmilzt.
Inhaltsverzeichnis
Gewinnung und Darstellung
Vanadium(II)-iodid kann durch Disproportionierung von Vanadium(III)-iodid bei 280 °C gewonnen werden:[4]
Eigenschaften
Physikalische Eigenschaften
Vanadium(II)-iodid besitzt eine oktaedrische Kristallstruktur, ähnlich der von Cadmiumiodid.[2]
Chemische Eigenschaften
Vanadium(II)-iodid ist ein starkes Reduktionsmittel, das sogar Stickstoff in Anwesenheit von Magnesiumhydroxid zu Hydrazin reduziert.[2]
Es löst sich in Wasser unter Bildung von [V(H2O)6]2+-Ionen:[2]
Einzelnachweise
- ↑ a b c Vanadium(II)-iodid auf webelements.com
- ↑ a b c d Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1550.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Lothar Kolditz: Anorganische Chemie Teil 2. VEB Deutscher Verlag der Wissenschaften, Berlin, 1980, S. 641
VanadiumhalogenideOxidationsstufe (II): Vanadium(II)-fluorid | Vanadium(II)-chlorid | Vanadium(II)-bromid | Vanadium(II)-iodid
Oxidationsstufe (III): Vanadium(III)-fluorid | Vanadium(III)-chlorid | Vanadium(III)-bromid | Vanadium(III)-iodid
Andere Oxidationsstufen: Vanadium(IV)-fluorid | Vanadium(IV)-chlorid | Vanadium(IV)-bromid | Vanadium(V)-fluorid
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Vanadium(III)-iodid — Kristallstruktur V3+ … Deutsch Wikipedia
Vanadium(II)-chlorid — Kristallstruktur V2+ … Deutsch Wikipedia
Vanadium(III)-chlorid — Kristallstruktur V3+ … Deutsch Wikipedia
Vanadium(III)-bromid — Kristallstruktur V3+ … Deutsch Wikipedia
Vanadium(IV)-fluorid — Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Vanadium(IV) fluorid Andere Namen Vanadiumtetrafluorid Vanadin(IV) fluorid Vanadintetrafluorid … Deutsch Wikipedia
Vanadium(III)-fluorid — Kristallstruktur Allgemeines Name Vanadium(III) fluorid … Deutsch Wikipedia
Vanadium(IV)-chlorid — Strukturformel Allgemeines Name Vanadium(IV) chlorid Andere Namen … Deutsch Wikipedia
Vanadium(V)-fluorid — Kristallstruktur V5+: F … Deutsch Wikipedia
Vanadium(II)-bromid — Kristallstruktur V2+ … Deutsch Wikipedia
Vanadium(II)-fluorid — Kristallstruktur V2+ … Deutsch Wikipedia


![\mathrm{V^{2+} + 6\ H_2O \longrightarrow [V(H_2O)_6]^{2+}}](2/5e253be3fdfcb5e498a90eee16d36982.png)