- Vanadium(III)-iodid
-
Kristallstruktur 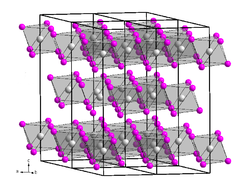
__ V3+ __ I− Allgemeines Name Vanadium(III)-iodid Andere Namen - Vanadiumtriiodid
- Vanadin(III)-iodid
- Vanadintriiodid
Verhältnisformel VI3 CAS-Nummer 15513-94-7 PubChem 84960 Kurzbeschreibung hygroskopischer, braunschwarzer Feststoff
Eigenschaften Molare Masse 431,655 g·mol−1 Aggregatzustand fest
Dichte 5,21 g·cm−3[1]
Schmelzpunkt sublimiert bei 80–100 °C[1]
Löslichkeit Zersetzung in Wasser[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Gefahr
H- und P-Sätze H: 314 EUH: keine EUH-Sätze P: 280-305+351+338-310 [3] EU-Gefahrstoffkennzeichnung [3] 
Ätzend (C) R- und S-Sätze R: 34 S: 22-26-27-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Vanadium(III)-iodid ist eine chemische Verbindung der Elemente Vanadium und Iod. Es ist ein braunschwarzer, hygroskopischer Feststoff, der bei 80–100 °C sublimiert[1].
Inhaltsverzeichnis
Gewinnung und Darstellung
Vanadium(III)-iodid kann aus den Elementen gewonnen werden[2]:

- Vanadium reagiert mit Iod beim Molverhältnis 2:3 zu Vanadium(III)-iodid.
Eigenschaften
Vanadium(III)-iodid kristallisiert im hexagonalen Kristallsystem in der Raumgruppe
 mit den Gitterparametern a = 692,5 pm und c = 1991 pm sowie 6 Formeleinheiten pro Elementarzelle. Es entspricht damit einer Bismut(III)-iodid-Struktur.[4]
mit den Gitterparametern a = 692,5 pm und c = 1991 pm sowie 6 Formeleinheiten pro Elementarzelle. Es entspricht damit einer Bismut(III)-iodid-Struktur.[4]Vanadium(III)-iodid ist oxidationsempfindlich und hygroskopisch. Es löst sich in Wasser unter Bildung von [V(H2O)6]3+-Ionen.[2]
Verwendung
Vanadium(III)-iodid ist ein Zwischenprodukt bei der Reinigung von Vanadium durch das Van-Arkel-de-Boer-Verfahren. Dabei wird das Vanadium(III)-iodid bei relativ niedrigen Temperaturen aus den Elementen gebildet, sublimiert und zersetzt sich an einem heißen Draht wieder in die Elemente.[5]
Einzelnachweise
- ↑ a b c Vanadium(III)-iodid auf webelements.com
- ↑ a b c Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1550.
- ↑ a b c Datenblatt Vanadium(III) iodide bei Sigma-Aldrich, abgerufen am 25. April 2011.
- ↑ Paper von Vanadiumiodiden der Louis Group
- ↑ Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1543.
VanadiumhalogenideOxidationsstufe (II): Vanadium(II)-fluorid | Vanadium(II)-chlorid | Vanadium(II)-bromid | Vanadium(II)-iodid
Oxidationsstufe (III): Vanadium(III)-fluorid | Vanadium(III)-chlorid | Vanadium(III)-bromid | Vanadium(III)-iodid
Andere Oxidationsstufen: Vanadium(IV)-fluorid | Vanadium(IV)-chlorid | Vanadium(IV)-bromid | Vanadium(V)-fluorid
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Vanadium(II)-iodid — Kristallstruktur V2+ … Deutsch Wikipedia
Vanadium(III)-chlorid — Kristallstruktur V3+ … Deutsch Wikipedia
Vanadium(III)-bromid — Kristallstruktur V3+ … Deutsch Wikipedia
Vanadium(III)-fluorid — Kristallstruktur Allgemeines Name Vanadium(III) fluorid … Deutsch Wikipedia
Vanadium(II)-chlorid — Kristallstruktur V2+ … Deutsch Wikipedia
Vanadium(II)-bromid — Kristallstruktur V2+ … Deutsch Wikipedia
Vanadium(II)-fluorid — Kristallstruktur V2+ … Deutsch Wikipedia
Vanadium(IV)-fluorid — Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Vanadium(IV) fluorid Andere Namen Vanadiumtetrafluorid Vanadin(IV) fluorid Vanadintetrafluorid … Deutsch Wikipedia
Vanadium(IV)-chlorid — Strukturformel Allgemeines Name Vanadium(IV) chlorid Andere Namen … Deutsch Wikipedia
Vanadium(IV)-bromid — Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Vanadium(IV) bromid Andere Namen Vanadiumtetrabromid Vanadin(IV) bromid Vanadintetrabromid … Deutsch Wikipedia
