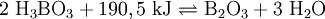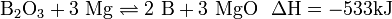- Dibortrioxid
-
Kristallstruktur 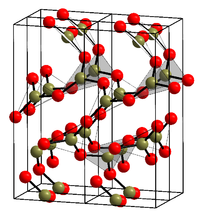
__ B3+ __ O2− Allgemeines Name Bortrioxid Andere Namen - Dibortrioxid
- Borsesquioxid
- Borsäureanhydrid
- Borsäureglas
- Boroxid
Verhältnisformel B2O3 CAS-Nummer 1303-86-2 Kurzbeschreibung farblose, glänzende, hygroskopische Kristalle Eigenschaften Molare Masse 69,62 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt 1860 °C[1]
Löslichkeit gering löslich in Wasser: 36 g·l−1 (25 °C)[3]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [4] 
Giftig (T) R- und S-Sätze R: 60-61 S: 53-45 LD50 3163 mg/kg[1] (oral, Maus)
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Bortrioxid oder Dibortrioxid ist eine chemische Verbindung der Elemente Bor und Sauerstoff mit der Summenformel B2O3.
Inhaltsverzeichnis
Geschichte
Bortrioxid war Ausgangspunkt zur ersten Darstellung von Bor. Im Jahre 1808 gelang erstmals die Darstellung von unreinem Bor aus Bortrioxid durch Reduktion mit Kalium. Das erste hochreine Bor wurde dann 1909 durch Reduktion von Bortrioxid mit Wasserstoff gewonnen.
Gewinnung und Darstellung
Glüht man Borsäure, so erhält man eine farblose, glasig-amorphe Masse (Boroxidglas), die schwierig zu kristallisieren ist:
Durch langsame Dehydratisierung von Borsäure bei 150–250 °C kann kristallines Bortrioxid hergestellt werden. Im Jahr 2000 wurden 5000 und 10.000 Tonnen Bortrioxid produziert.[5]
Eigenschaften
Bortrioxid reagiert sauer, ist hygroskopisch und bildet Borsäure bei Kontakt mit Wasser. Bei Reduktion mit Magnesium, Kalium, Wasserstoff und anderen entsteht Bor.
Verwendung
Bortrioxid ist ein Ausgangsstoff zur Herstellung weiterer Borverbindungen (z.B. reinem Bor, Borkarbid, Methylborate durch Auflösung in Methanol, Diboran durch Hydrierung). Praktische Verwendung findet es als Flussmittel bzw. Bestandteil (Borsilikatglas, Borphosphatglas) in Emails und Gläsern. In heißgepresster Bornitrid-Keramik vermag es in Mengen von 2–6 % als Bindemittel zu fungieren.
Quellen
- ↑ a b c d Sicherheitsdatenblatt (alfa-aesar)
- ↑ Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ Eintrag zu Bortrioxid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 28.12.2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 1303-86-2 im European chemical Substances Information System ESIS
- ↑ ESIS: IUCLID Datasheet
Wikimedia Foundation.