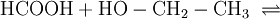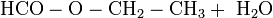- Ethylformiat
-
Strukturformel 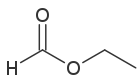
Allgemeines Name Ameisensäureethylester Andere Namen - IUPAC: Ethylmethanoat
- Ameisensäureester
- Ameisensäurevinester
- Ethylformiat
- Formosol
- Methenyl
- Rumether
Summenformel C3H6O2 CAS-Nummer 109-94-4 Kurzbeschreibung Leichtentzündliche farblose Flüssigkeit Eigenschaften Molare Masse 74,08 g·mol−1 [1] Aggregatzustand flüssig
Dichte 0,92 g·cm−3 [1]
Schmelzpunkt −80 °C [1]
Siedepunkt 54 °C [1]
Dampfdruck Löslichkeit gut wasserlöslich (105 g/1) [1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Leicht-
entzündlichGesundheits-
schädlich(F) (Xn) R- und S-Sätze R: 11-20/22-36/37 S: (2)-9-16-24-26-33 MAK WGK 1 (schwach wassergefährdend) [1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Ameisensäureethylester (IUPAC : Ethylmethanoat, auch Ethylformiat) ist der Ester aus Ethanol (C2H5OH) und Ameisensäure (HCOOH). Er hat einen typischen Rumgeruch (Arrak).
Inhaltsverzeichnis
Vorkommen
Als natürlicher Aromastoff kommt Ameisensäureethylester in vielen verschiedenen Pflanzen vor. Es wurde auch als eines der kompliziertesten Molekülen im Weltall, genauer in der Sternentstehungsregion Sagittarius B2 in der Nähe des Milchstraßenzentrums, gefunden.[3]
Gewinnung und Darstellung
Seine Darstellung ist aus Ameisensäure und Ethanol durch Veresterung unter Wasserabspaltung möglich:
Die Einstellung des Gleichgewichts wird durch Zusatz von starken Säuren beschleunigt und durch Entfernen des bei der Reaktion entstehenden Wassers auf die rechte Seite verlagert.
Eigenschaften
Physikalische Eigenschaften
Ethylformiat ist eine klare, leichtflüchtige und leichtentzündliche Flüssigkeit von charakteristischem Geruch. Die Dämpfe sind mit Luft im Bereich von 2,7 Vol.-% (80 g·m−3) bis 16,5 Vol.-% (500 g·m−3) explosiv.
Chemische Eigenschaften
Der Ester kann durch Reaktion mit Wasser in Umkehrung der Bildungsreaktion verseift, d. h. hydrolysiert werden. Die Hydrolyse kann durch Säuren katalysiert werden und verläuft dann in genauer Umkehrung der Veresterungsreaktion; es entstehen wieder Ethanol und Ameisensäure. Bei der basischen Hydrolyse erhält man dagegen Ethanol und ein Salz der Ameisensäure, ein Formiat.
Verwendung
Ethylformiat wird vorwiegend zur Herstellung künstlicher Arrak- und Rumessenzen verwendet. Weiterhin dient es als Fungizid für Getreide und Tabak. Der Einsatz von Ethylformiat im Vorratsschutz wurde zumindest diskutiert.[4] In Deutschland, Österreich und der Schweiz besteht keine Zulassung von Ethylformiat als Pflanzenschutzmittel.[5] Ethylformiat dient als Zwischenprodukt bei verschiedenen organischen Synthesen (Formylierung). In der Industrie wird es auch als Lösemittel für Nitrocellulose und Celluloseacetat eingesetzt.
Sicherheitshinweise
Der Ester ist sehr leicht entzündlich und reagiert auch mit vielen Oxidationsmitteln. Dabei können gefährliche Stoffe wie Ameisensäure, Formaldehyd und Kohlenstoffmonoxid entstehen. Ameisensäureethylester kann sowohl über die Haut, als auch die Atemwege aufgenommen werden, wobei Reizung von Augen, Schleimhäuten und Atemwegen auftreten. Höhere Konzentrationen oder Aufnahme über einen längeren Zeitraum können Schädigungen des Zentralnervensystems und der Lunge hervorrufen.[1]
Quellen
- ↑ a b c d e f g h i j Eintrag zu CAS-Nr. 109-94-4 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 30. März 2008 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 109-94-4 im European chemical Substances Information System ESIS
- ↑ Wissenschaft-aktuell: Komplexe Moleküle im All
- ↑ Institut für Vorratsschutz Berlin
- ↑ Nationale Pflanzenschutzmittelverzeichnisse: Schweiz, Österreich, Deutschland; abgerufen am 24. Januar 2009
Weblinks
Wikimedia Foundation.