- Genistein
-
Strukturformel 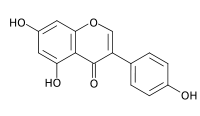
Allgemeines Freiname Genistein Andere Namen - 5,7-Dihydroxy- 3-(4-hydroxyphenyl) chromen-4-on(IUPAC)
- 4',5,7-Trihydroxyisoflavon
Summenformel C15H10O5 CAS-Nummer 446-72-0 PubChem 5280961 DrugBank EXPT01582 Kurzbeschreibung farbloses Pulver[1]
Arzneistoffangaben Wirkstoffklasse Eigenschaften Molare Masse 270,24 g·mol−1 Schmelzpunkt Löslichkeit löslich in Ethanol und DMSO[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Achtung
H- und P-Sätze H: 302 EUH: keine EUH-Sätze P: keine P-Sätze [1] EU-Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22 S: 22-45 LD50 500 mg·kg−1 (Maus, oral)[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Genistein ist ein Phytoöstrogen aus der Gruppe der Isoflavonoide, das zusammen mit Genistin in der Sojabohne und dem Rotklee vorkommt.
Pharmakologie
Genistein wird über die Nahrung aufgenommen und lässt sich im Serum von Menschen und Tieren nachweisen.
Wie andere Östrogene führt auch Genistein zu einer beschleunigten Kapazitation der Samenzellen im weiblichen Genitaltrakt – derzeit wird allerdings auch untersucht, ob die Fertilität durch eine vorzeitige Akrosomreaktion nicht doch herabgesetzt wird. Dies mag als Beispiel dafür gelten, dass auch pflanzliche Stoffe neben ihren gewünschten Eigenschaften unerwünschte Nebenwirkungen aufweisen.
Es gibt mehrere Hinweise darauf, dass Genistein, ebenso wie ein anderes Isoflavon (Daidzein), die Transkription des Enzyms Catechol-O-Methyltransferase (COMT) herunterfährt, die normalerweise Estradiol abbaut.[3]
In der Tumorforschung wird nebenbei auch untersucht, ob der Stoff bzw. die Anwendung von z.B. Sojaextrakten eine positive Wirkung auf das Tumorwachstum hat, da Genistein die durch FGF-2-induzierte Angiogenese aufgrund der Hemmung der Tyrosinkinase, uPA (Urokinase) und Hochregulierung der PAI-1 inhibiert.
Einzelnachweise
- ↑ a b c d e Datenblatt Genistein bei Sigma-Aldrich, abgerufen am 3. April 2011.
- ↑ a b Datenblatt Genistein bei Carl Roth, abgerufen am 14. Dezember 2010.
- ↑ Lehmann L, Jiang L, Wagner J: Soy isoflavones decrease the catechol-O-methyltransferase-mediated inactivation of 4-hydroxyestradiol in cultured MCF-7 cells. In: Carcinogenesis. 29, Nr. 2, Februar 2008, S. 363–370. doi:10.1093/carcin/bgm235. PMID 18192686.

Bitte den Hinweis zu Gesundheitsthemen beachten!
Wikimedia Foundation.
