- 2,4,6-Triamino-1,3,5-triazin
-
Dieser Artikel behandelt die chemische Verbindung Melamin, nicht das Hautpigment Melanin. - Cyanursäuretriamid
- 2,4,6-Triamino-1,3,5-triazin
- Holzwerkstoffleime: Für Standardprodukte (etwa Spanplatten im Möbelbau) werden aus preislichen Gründen reine Harnstoffharze verwendet, für Anwendungen, die erhöhte Anforderungen bezüglich Feuchtebeständigkeit haben, wird jedoch Melamin als Bestandteil in hochwertigen Harzklebesystemen verwendet (etwa Melamin-Harnstoff-Formaldehyd-Harze = MUF).
- Tränkharze: Als MF-Tränkharz dient es auch zur Verklebung von Dekorpapieren auf Trägerplatten (wie beispielsweise Spanplatten). Die meist bedruckten oder gefärbten Papiere werden mit Melaminharz getränkt, getrocknet und später unter Druck und erhöhter Temperatur mit dem Trägermaterial verbunden. Die dabei entstehenden Oberflächen erhalten dadurch auch noch eine gute Haltbarkeit und können so beispielsweise als Arbeitsplatten in Küchen verwendet werden.
- Unter dem Handelsnamen Basotect (BASF) wird Melaminharzschaum als nichtbrennbares Polstermaterial in Flugzeug- und Kinositzen, als akustischer Absorber für (Heim-)Kinos, Tonstudios und schalltote Räume verwendet. Auch in der Bautechnik findet es in Form von Blöcken Verwendung, wie etwa in Gaststätten, wo es die Sprachverständlichkeit verbessern kann und für eine akustisch „wärmere“, behagliche Atmosphäre sorgt. Zudem ist hier auch die thermische und akustische Dämmwirkung (z. B. in Discotheken) erwünscht. Auch zur Verwendung als Schmutzradierer wird das Produkt angeboten.
- Das Salz von Melamin mit Cyanursäure Melamincyanurat sowie auch Melaminpolyphosphat werden als Flammschutzmittel eingesetzt. Melamincyanurat ist dabei bis etwa 320 °C, Melaminpolyphosphat bis zu 350 °C stabil.[5]
- ↑ a b c d e f g Eintrag zu Melamin in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 11. Januar 2008 (JavaScript erforderlich)
- ↑ a b c Toxicology and Applied Pharmacology. Vol. 72, Pg. 292, 1984.
- ↑ Eintrag zu Melamin im European chemical Substances Information System ESIS
- ↑ Romer Labs - AgraQuant® Melamine ELISA Test Kit
- ↑ Flame Retardants Center: Melamine Compounds
- ↑ Stiftung Warentest: Melamin in Milchprodukten : Keine Panik, Meldung vom 01. Oktober 2008
- ↑ Melamin Salze, Bereich Makromolekulare Chemie der TU Wien
- ↑ Interim Melamine and Analogues Safety/Risk Assessment, U.S. Food and Drug Administration, 25.05.2007
- ↑ MSNBC: Human, pet food makers checked for melamine 3. Mai 2007
- ↑ Science Daily: Pet Food Recall: How Melamine Impairs Kidney Function
- ↑ Cianciolo et al.: Clinicopathologic, histologic, and toxicologic findings in 70 cats inadvertently exposed to pet food contaminated with melamine and cyanuric acid. J Am Vet Med Assoc. 2008 Sep 1;233(5):729-37. PMID 18764706
- ↑ "Vertuscht und verschwiegen: Melamin-Skandal weitet sich aus" (Zeit Online vom 02. Dezember 2008)
- ↑ „Melamin in Milchprodukten in China und Hongkong entdeckt“ (AFP-Meldung vom 18. September 2008)
- ↑ Melamin-Milch auch in der Slowakei entdeckt www.heute.de, 4. Oktober 2008
- ↑ RP Online: Melamin-Skandal weitet sich aus: Chemikalie auch im Weihnachtsgebäck?, 2. Dezember 2008
- ↑ Gericht verhängt Todesstrafen im Milchpulver-Skandal Spiegel Online, 22. Januar 2009
- Anthony Kai-ching Hau, Tze Hoi Kwan, Philip Kam-tao Li: Melamine toxicity and the kidney. In: Journal of the American Society of Nephrology: JASN. 20, Nr. 2, 2009-02, S. 245-50. doi:10.1681/ASN.2008101065 (Volltext frei ab 02/2010)
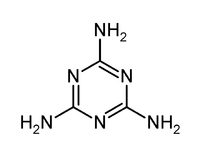
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
 |
|||||||
| Allgemeines | |||||||
| Name | Melamin | ||||||
| Andere Namen |
|
||||||
| Summenformel | C3H6N6 | ||||||
| CAS-Nummer | 108-78-1 | ||||||
| PubChem | 7955 | ||||||
| Kurzbeschreibung | weißes Pulver | ||||||
| Eigenschaften | |||||||
| Molare Masse | 126,12 g·mol−1 | ||||||
| Aggregatzustand |
fest |
||||||
| Dichte |
1,574 g·cm−3 (20 °C) [1] |
||||||
| Schmelzpunkt | |||||||
| Dampfdruck |
< 0,001 mbar (20 °C) [1] |
||||||
| Löslichkeit |
in Wasser 3,2 g·l−1 [1] |
||||||
| Sicherheitshinweise | |||||||
|
|||||||
| LD50 | |||||||
| WGK | 1 (schwach wassergefährdend) [1] | ||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Melamin (2,4,6-Triamino-s-triazin), ein weißes Pulver, ist eine heterocyclische aromatische Verbindung. Im Handel und alltäglichen Sprachgebrauch wird der Begriff auch für einen Kunststoff aus der Gruppe der Duroplaste, ein Aminoplast verwendet.
Inhaltsverzeichnis |
Gewinnung und Darstellung
Justus von Liebig stellte 1834 Melamin aus Kaliumthiocyanat und Ammoniumchlorid erstmals dar. Die erste kommerzielle Herstellung fand 1930 statt, worauf Bedeutung und Menge des jährlich hergestellten Melamins stark anstiegen. Früher spielte die Trimerisierung von Cyanoguanidin eine Rolle.
Melamin wird heute technisch durch Trimerisierung von Harnstoff gewonnen. Es existieren Hochdruck- (> 8 MPa) und Niederdruckverfahren (ca. 1 MPa). Es ist ein High Production Volume Chemical (HPV).[3] Bedeutende Hersteller sind unter anderem BASF, DSM Melamin, Agrolinz Melamine International GmbH (AMI) und Zakłady Azotowe Puławy (ZAP). Für den europäischen Markt werden auch Importe aus Asien, insbesondere aus der Volksrepublik China, immer bedeutender.
Anlagen zur Herstellung von Melamin sind meist direkt an solche zur Harnstoffherstellung angebunden.
Als Nebenprodukte entstehen polycyclische Verbindungen wie Melam und Melem wie auch Verbindungen mit Hydroxygruppen statt Aminogruppen wie Ammelin mit einer OH-Gruppe, Ammelid mit zwei OH-Gruppen und Cyanursäure mit drei OH-Gruppen, die allerdings im fertigen technischen Produkt meist nur mehr zu < 0,1 % vorkommen.
Eigenschaften
Physikalische Eigenschaften
Melamin beginnt sich beim Schmelzen (ab etwa 350 °C) zu zersetzen. Es ist in kaltem Wasser wenig, in heißem gut löslich.
Chemische Eigenschaften
Die drei reaktiven Amin-Gruppen ermöglichen eine Vielzahl chemischer Reaktionen, von denen die Reaktion mit Formaldehyd zu sogenannten Methylol-Melaminen die wirtschaftlich bedeutendste ist (siehe Abbildung).
Durch die Reaktionsbedingungen und das molare Verhältnis von Melamin zu Formaldehyd lässt sich das Gleichgewicht von Melamin über Mono-, Di-, Tri-, Tetra-, Penta- bis zu Hexamethylolmelamin beeinflussen.

Bei der Tränkharz-Herstellung (sowie auch anderen sogenannten MF-Harzen) wird das Reaktionsprodukt weiter kondensiert, wobei höhermolekulare Verbindungen entstehen.
Darüber hinaus bildet Melamin wasserlösliche Salze mit vielen Mineralsäuren und organischen Säuren.
Analytik
Die qualitative und quantitative Bestimmung von Melamin bzw. Melamin-Metaboliten in komplexen Matrices wie z.B. Lebensmitteln erfolgt zuverlässig mit hoher Spezifität und Sensitivität mit den Methoden der HPLC und der Kopplung der HPLC mit der Massenspektrometrie. Des Weiteren wurde von Romer Labs eine Screeningmethode basierend auf dem ELISA-Prinzip entwickelt. Die Testmethode ist für Tierfutter, Weizengluten, Milch und Milchpulver nach den Kriterien der GIPSA zugelassen.[4]
Verwendung
Industrie
Der überwiegende Teil von Melamin wird zu Aminoplast-Kunstharzen unter der Bezeichnung Melaminharz verarbeitet:
Des Weiteren existieren noch eine Vielzahl anderer, mengenmäßig weniger bedeutende Anwendungen:
Putzmittel
Offenporiger Schaum aus Melaminharz wird auch als „Schmutzradierer“, etwa der Handelsmarken „Meister Proper“[6], „Meiko“ oder „Oetex“ genutzt. Die Reinigungswirkung beruht auf den abrasiven Harzpartikeln, die beim Reiben entstehen. Die Partikel werden, zusammen mit den Schmutzpartikeln, vom Schwamm aufgenommen. Der Schwamm verbraucht sich somit beim Reinigen.
Toxikologie
Die letale orale Dosis LD50 liegt für Ratten bei 3161 mg/kg, für Mäuse 3296 mg/kg.[2] Die orale Aufnahme hoher Mengen führt bei verschiedenen Tierarten zur Bildung von Kristallen im Urin und Harnblasensteinen. Bei männlichen Ratten wurde eine erhöhte Inzidenz von Harnblasentumoren beobachtet. Es kann bei langfristiger hochdosierter Einnahme zum Tod durch Nierenversagen kommen. Das dabei beobachtete Auskristallisieren in den Harnwegen beruht allerdings nicht auf Melamin, sondern auf dessen Salzen, z. B. mit Glykolsäure.[7] Die Anreicherung in der Nahrungskette gilt als hochgradig unwahrscheinlich.[8]
Bei der Gabe hoher Dosen im Letalbereich an Mäuse und Ratten traten als Symptome Augentränen, Atemstörungen, Zittern, Kreislaufstörungen und Lähmung der Vorderextremitäten auf.[1]
Missbrauch in Tierfutter und Lebensmitteln
In China wurde Melamin 2006 dazu verwendet, eine für die USA bestimmte Lieferung von Weizengluten – ein Bestandteil von Haustierfutter – zu strecken, um einen höheren Proteingehalt vorzutäuschen. Die Fütterung führte zum Tod von Haustieren durch Nierenversagen, und 2007 wurde ein landesweiter Rückruf des Futters eingeleitet.[9][10] Zur Pathophysiologie von Melamin bei Hauskatzen wurde inzwischen eine umfassende wissenschaftliche Untersuchung vorgelegt.[11]
Um die illegale Streckung von Milchpulver und anderen Milchprodukten durch bislang noch unbekannte Stoffe, aber auch Wasser, zu verdecken, wurde von chinesischen Molkereien und Babynahrungsherstellern dem Milchpulver Melamin zugesetzt. Dieses Verfahren ließ den Stickstoffgehalt höher als normal erscheinen. Die Bestimmung des Stickstoffgehalts nach Kjeldahl wird in der Lebensmittelanalytik als einfache, aber unspezifische Methode zur Ermittlung des Proteingehalts verwendet. Die für Nieren giftige Wirkung von Melamin führte 2008 in China zum Tod von sechs Säuglingen und durch Nierenstein-Bildung zur Erkrankung von rund 294.000 Kindern.[12] Melamin wurde außerdem in Milchfertigprodukten und gewöhnlicher Flüssigmilch nachgewiesen.[13]
Am 25. September 2008 verbot die Kommission der Europäischen Union die Einfuhr aller Erzeugnisse für Säuglinge und Kleinkinder aus China, welche Milchanteile enthalten. Dennoch mussten Anfang Oktober 2008 sowohl in Österreich als auch in der Slowakei mit Melamin belastete Milchgetränke aus dem Verkehr gezogen werden.[14] Ende 2008 fand das baden-württembergische Verbraucherministerium in Hirschhornsalz aus China Spuren von Melamin. Die Behörden starteten eine Rückrufaktion der betroffenen Ware, die nicht dem Reinheitsgebot nach dem Lebensmittelrecht entspricht.[15]
Im ersten Prozess um die vergiftete Babynahrung verurteilte ein Gericht in der Provinz Hebei im Januar 2009 drei Angeklagte zum Tode. Sie wurden für schuldig befunden, an der Herstellung von verseuchtem Milchpulver beteiligt gewesen zu sein. Das Gericht verhängte außerdem für weitere Angeklagte Haftstrafen zwischen fünf und 15 Jahren. [16]
Einzelnachweise
Übersichtsarbeiten
Weblinks
Wikimedia Foundation.
