- Ammoniumcitrat
-
Strukturformel 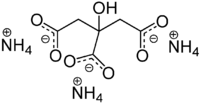
Allgemeines Name Ammoniumcitrat, Andere Namen - Triammoniumcitrat
- Ammoniumcitrat tribasisch
- E 380
- 2-Hydroxypropan-1,2,3-tricarbonsäure Triammoniumsalz
Summenformel C6H17N3O7 CAS-Nummer 3458-72-8 PubChem 18954 Kurzbeschreibung farblose, kristalline Substanz[1]
Eigenschaften Molare Masse 243,22 g·mol−1 Aggregatzustand fest
Dichte 1,48 g·cm−3 (20 °C)[2]
Schmelzpunkt Löslichkeit leicht löslich in Wasser[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [3] EU-Gefahrstoffkennzeichnung [1] 
Reizend (Xi) R- und S-Sätze R: 36/37/38 S: 26-37 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Ammoniumcitrat ist das Ammoniumsalz der Citronensäure. Es besteht aus drei Ammoniumionen (NH4+) und dem Citration (C6H5O73−) und bildet farblose Kristalle, die sich gut in Wasser lösen. Neben Triammoniumcitrat existiert ebenfalls noch Monoammoniumcitrat (C6H8O7)2H3N (CAS: 3012-65-5).
Synthese
Ammoniumcitrat lässt sich durch die Neutralisation von Ammoniak mit Citronensäure gewinnen:
Verwendung
Ammoniumcitrat ist in der EU als Lebensmittelzusatzstoff E 380 zugelassen. Es findet als Säureregulator und Farbstabilisator unter anderem in Limonaden, Konfitüren, Frucht- und Gemüsekonserven, Backwaren, Fertigsuppen und Tiefkühlfisch Verwendung.
Einzelnachweise
- ↑ a b c Datenblatt Ammoniumcitrat bei AlfaAesar, abgerufen am 26. März 2010 (JavaScript erforderlich).
- ↑ Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.5. Georg Thieme Verlag KG, Stuttgart 2009.
- ↑ a b c Datenblatt Ammoniumcitrat bei Sigma-Aldrich, abgerufen am 9. März 2011.
Kategorien:- Reizender Stoff
- Ammoniumverbindung
- Citrat
- Säuerungsmittel
Wikimedia Foundation.


