- Kaliumchromat
-
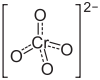
Strukturformel 
Allgemeines Name Kaliumchromat Andere Namen Dikaliumchromat, Chromsaures Kalium
Summenformel K2CrO4 CAS-Nummer 7789-00-6 PubChem 24597 Kurzbeschreibung zitronengelber, kristalliner Feststoff[1]
Eigenschaften Molare Masse 194,19 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Siedepunkt 1000 °C[1]
Löslichkeit Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 


Gefahr
H- und P-Sätze H: 350i-340-319-335-315-317-410 EUH: keine EUH-Sätze P: 201-280-273-308+313-305+351+338-302+352 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 49-46-36/37/38-43-50/53 S: 53-45-60-61 MAK aufgehoben, da karzinogen[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Kaliumchromat ist ein Kaliumsalz der Chromsäure (H2CrO4) mit der Summenformel K2CrO4. Es ist ein nicht brennbarer, zitronengelber, giftiger und umweltgefährlicher Feststoff. Das Salz ist ein starkes Oxidationsmittel und wirkt ätzend auf Haut und Schleimhäute.
Inhaltsverzeichnis
Gewinnung und Darstellung
Durch die Reaktion von Kaliumcarbonat und Kaliumdichromat wird Kaliumchromat hergestellt.
Eigenschaften
Wasserfreies Kaliumchromat bildet zitronengelbe, prismenförmige Kristalle, welche sich oberhalb von 670°C in eine rote hexagonale α-Modifaktion umwandeln.
Bei Berührung mit brennbaren Stoffen ist das Salz feuergefährlich.
Verwendung
Kaliumchromat wurde fast vollständig durch das preiswertere Natriumchromat ersetzt und wird nur noch für sehr spezifische Anwendungen, wie beispielsweise in der Fotografie oder als Indikator bei der Titration von Natriumchlorid nach Mohr verwendet (DAB7).
Sicherheitshinweise
Kaliumchromat ist giftig und umweltgefährlich. Es führt zu Reizung und Schädigung von Haut und Schleimhäuten und schädigt Nieren, Blut und Leber. Kaliumchromat wirkt weiterhin mutagen und karzinogen.
Kaliumchromat verursacht an verletzten Hautstellen schlecht heilende Wunden.
Nachweis
Das Chromat-Anion (CrO42-) lässt sich in wässriger Lösung mit Metallkationen wie Ba2+ Pb2+, Hg22+ als, je nach Kation gelber bis braunroter, Niederschlag ausfällen:
Es ist dabei zu beachten, dass in sehr sauren Lösungen das Chromat-Dichromat-Gleichgewicht zunehmend zum Dichromat verschoben ist.
Einzelnachweise
- ↑ a b c d e f g Eintrag zu Kaliumchromat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 25.8.2007 (JavaScript erforderlich)
- ↑ Helmut Sitzmann in: Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b Eintrag zu CAS-Nr. 7789-00-6 im European chemical Substances Information System ESIS (ergänzender Eintrag)
Kategorien:- Krebserzeugender Stoff
- Erbgutverändernder Stoff
- Sensibilisierender Stoff
- Umweltgefährlicher Stoff
- Chromat
- Kaliumverbindung
Wikimedia Foundation.




