- Na2SO4
-
Strukturformel 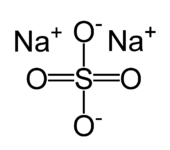
Allgemeines Name Natriumsulfat Andere Namen - Dinatriumsulfat
- E 514
- Glaubersalz (Decahydrat)
Summenformel Na2SO4 CAS-Nummer 7757-82-6 ATC-Code Kurzbeschreibung farb- und geruchlose Kristalle Eigenschaften Molare Masse 142,04 g·mol−1 Aggregatzustand fest
Dichte 2,70 g·cm–3 (20 °C)[1]
Schmelzpunkt Siedepunkt Zersetzung ab 890 °C[1]
Löslichkeit gut in Wasser: 170 g/l, bei 20 °C[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Natriumsulfat (Na2SO4, veraltete Bezeichnung Schwefelsaures Natron) ist ein Natriumsalz der Schwefelsäure und setzt sich aus zwei Natriumkationen (Na+) und dem Sulfatanion (SO42-) zusammen. Das Dekahydrat (Na2SO4 · 10 H2O) wird nach dem Chemiker Johann Rudolph Glauber auch Glaubersalz genannt. Auch Karlsbader Salz, das durch Eindampfen von Karlsbader Mineralwasser gewonnen wird, besteht hauptsächlich aus Natriumsulfat-Dekahydrat und wird wie Glaubersalz als Abführmittel eingesetzt.
Inhaltsverzeichnis
Geschichte
Natriumsulfat wurde 1625 von dem Chemiker und Apotheker Johann Rudolph Glauber hergestellt und beschrieben und wird daher auch als Glaubersalz bezeichnet. Er selbst nannte das von ihm entdeckte Salz auch Sal mirabilis und Mirabili.
Gewinnung und Darstellung
Natriumsulfat wird nur selten aus natürlichen Mineralien abgebaut, da es häufig als Nebenprodukt in der chemischen Industrie bei Reaktionen, bei denen Schwefelsäure mit Natronlauge neutralisiert wird, anfällt. Eine weitere Möglichkeit zur technischen Darstellung besteht in der Umsetzung von Steinsalz (NaCl) mit Schwefelsäure zwecks Gewinnung von Salzsäure mit Natriumsulfat als Nebenprodukt (bei 800 °C):
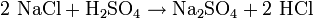
- Natriumchlorid und Schwefelsäure reagieren zu Natriumsulfat und Chlorwasserstoff.
Natriumsulfat lässt sich im Labor durch folgende Reaktionen herstellen:
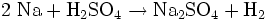
- Natrium und Schwefelsäure reagieren zu Natriumsulfat und Wasserstoff.
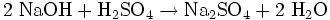
- Bei der Neutralisation von Natronlauge mit Schwefelsäure entstehen Natriumsulfat und Wasser.
Eigenschaften
Das wasserfreie Natriumsulfat schmilzt bei 884 °C, ist hygroskopisch und gut in Wasser unter Erwärmung (Lösungswärme) löslich. Dagegen löst sich das Dekahydrat unter starker Abkühlung, bedingt durch den sogenannten Entropie-Effekt. Natriumsulfat-Dekahydrat ist Bestandteil vieler Mineralwasser und schmilzt ab etwa 32 °C langsam in seinem eigenen Kristallwasser. Aus dieser an wasserfreiem Natriumsulfat übersättigten Lösung scheidet sich das wasserfreie Salz ab.
Verwendung
Natriumsulfat wird in Waschmitteln als Füllstoff, in der Medizin als Abführmittel, bei der Zellstoffgewinnung (Sulfatverfahren) sowie in der Glas-, Textil- und Farbindustrie eingesetzt. Geglühtes, kristallwasserfreies Natriumsulfat wird im Labor zur Trocknung von organischen Lösungsmitteln verwendet. Das Natriumsulfat-Dekahydrat (Glaubersalz) wird als Abführmittel und als Latentwärmespeichermaterial verwendet.
In der Lebensmitteltechnologie dient es als Festigungsmittel, Säureregulator und Trägersubstanz. Natriumsulfat und Natriumhydrogensulfat sind in der EU als Lebensmittelzusatzstoff der Nummer E 514 ohne Höchstmengenbeschränkung (quantum satis) für Lebensmittel allgemein zugelassen.[2]
Quellen
- ↑ a b c d e Eintrag zu Natriumsulfat in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 25.4.2008 (JavaScript erforderlich)
- ↑ Natriumsulfate - Datenbank Zusatzstoffe
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.

