- PMSF
-
Strukturformel 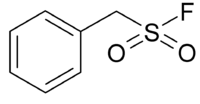
Allgemeines Name Phenylmethylsulfonylfluorid Andere Namen - α-Toluolsulfonylfluorid
- Benzylsulfonylfluorid
- Phenylmethansulfonylfluorid
Summenformel C7H7FO2S CAS-Nummer 329-98-6 Kurzbeschreibung farblose bis hellgelbe Kristalle Eigenschaften Molare Masse 174,2 g·mol−1 Aggregatzustand fest
Schmelzpunkt 92–93 °C [1]
Löslichkeit gut löslich in Alkoholen und DMSO; nicht stabil in wässriger Lösung [1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Giftig (T) R- und S-Sätze R: 25-34 S: 26-36/37/39-45 LD50 200 mg·kg−1 (Maus, oral) [2]
WGK 3 [2] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Phenylmethylsulfonylfluorid (PMSF) ist eine chemische Verbindung, die als Protease-Inhibitor vor allem in der Molekularbiologie Anwendung findet.
Inhaltsverzeichnis
Biochemische Eigenschaften
PMSF inhibiert vor allem Serin-Proteasen (Chymotrypsin, Trypsin und Thrombin) sowie die Cystein-Protease Papain, aber auch die Acetylcholinesterase von Säugetieren, allerdings weniger effektiv als DFP. Die Substanz ist daher giftig (LD50 < 500 mg/kg) und steht im Verdacht, Krebs zu erzeugen.
Die inhibitorische Wirkung auf Cystein-Proteasen ist durch reduzierte Thiole umkehrbar, weshalb für die Anwendung im molekularbiologischen Labor auf den Einsatz von DTT oder Mercaptoethanol im Lysis-Puffer verzichtet und nach Alternativen (entweder für PMSF oder für ein Reduktionsmittel) gesucht werden sollte.
Hohe Salzkonzentrationen schränken die inhibitorische Wirkung ebenfalls ein.
Verwendung
PMSF wird (oft zusammen mit anderen Proteasehemmern) verwendet, um beim Aufschluss von Geweben und kultivierten Zellen unerwünschten Proteinabbau durch ebenfalls im Lysat befindliche Proteasen zu verhindern. PMSF wird erst kurz vor Gebrauch zugefügt, denn wässrige Lösungen sind instabil und degradieren rapide. So besitzt es in wässriger Lösung bei einem pH-Wert von 7 nur eine Halbwertzeit von 110 min, die mit basischer werdendem, aber bei Proteinextraktionen häufig gebrauchtem, Milieu weiter abnimmt (z.B. 55 min bei pH 7,5 bzw. 35 min bei pH 8). Stammlösungen werden aus dem Feststoff meist in Isopropanol, Methanol oder auch in DMSO oder Maiskeimöl hergestellt; PMSF löst sich ebenfalls gut in Ethanol, der jedoch wegen seiner Hygroskopie häufig Wasser enthält und daher hydrolytisch und damit inaktivierend auf PMSF wirken kann, und somit selten und dann auch nur absolut und nicht vergällt als Lösemittel verwendet wird. Die Lagerung der Lösungen erfolgt abgedunkelt bei −20 °C – für kürzere Lagerung (mind. 9 Monate) ist auch Kühlschranktemperatur (2–8 °C) ausreichend.
Alternativen
4-(2-Aminoethyl)-benzensulfonylfluorid (AEBSF), auch Pefabloc SC® genannt, ist ein stabilerer, wasserlöslicher Serin-Proteaseninhibitor.
Quellen
- ↑ a b c Eintrag zu Phenylmethansulfonylfluorid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 12. Mai 2008 (JavaScript erforderlich)
- ↑ a b PMSF bei Sigma-Aldrich
Weblinks
Wikimedia Foundation.
