- Taxol
-
Strukturformel 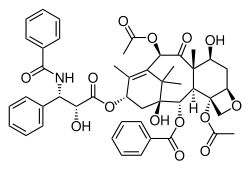
Allgemeines Freiname Paclitaxel Andere Namen - Abraxen
- Taxol
Summenformel C47H51NO14 CAS-Nummer 33069-62-4 PubChem 36314 ATC-Code L01CD01
DrugBank APRD00259 Kurzbeschreibung weißliches, kristallines Pulver Arzneistoffangaben Wirkstoffklasse Fertigpräparate - Taxol® (D)
- Ebetaxel® (A)
- Paclitaxel Teva® (CH)
Eigenschaften Molare Masse 853,92 g·mol−1 Schmelzpunkt Siedepunkt Zersetzung oberhalb des Schmelzpunktes
Löslichkeit abhängig von der Modifikation und der Messmethode werden Löslichkeiten von ca. 0,1 mg·l−1 bis zu 30 mg·l−1 in Wasser angegeben. [2]
Sicherheitshinweise Gefahrstoffkennzeichnung [1]
T
GiftigR- und S-Sätze R: 36/37-41-46-60 S: 22-26-36/37/39-45 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Paclitaxel (Markenname Taxol®) ist eine in der Pazifischen Eibe (Taxus brevifolia) vorkommende Substanz aus der Gruppe der Taxane. Paclitaxel wird als Arzneistoff in der Medizin zur Behandlung verschiedener Krebsarten (z. B. Brustkrebs) eingesetzt.
Inhaltsverzeichnis
Eigenschaften
Paclitaxel ist bei Raumtemperatur ein farbloser Feststoff. In Wasser ist es kaum löslich. Es gibt mindestens drei kristalline Formen, eine davon ist ein Dihydrat. Es sind auch glasig erstarrte Modifikationen mit einem Glasübergang um 152 °C beschrieben. Die verschiedenen Angaben zur Löslichkeit können auf das Vorliegen unterschiedlicher Kristallstrukturen bzw. die Bildung eines schwerer löslichen Dihydrates in wässriger Lösung zurückgeführt werden.
Gewinnung
Paclitaxel kann aus der Rinde der Pazifischen Eibe (Taxus brevifolia) gewonnen werden. Da diese Eibenart nur eine sehr geringe Verbreitung hat und der Taxolgehalt sehr gering ist, kann sie nicht den Weltbedarf an Paclitaxel decken. Seit einigen Jahren wird daher Paclitaxel überwiegend partialsynthetisch aus dem in Nadeln der Europäischen Eibe (Taxus baccata) vorkommenden Baccatin III gewonnen. Dies geschieht nach dem Ojima-Holton-Verfahren, das unter anderem von Iwao Ojima entwickelt wurde.
Eine Totalsynthese von Paclitaxel wurde erstmals im Jahre 1994 von K. C. Nicolaou beschrieben, fand jedoch keine industrielle Verwendung.
Neben der pazifischen Eibe wurde auch nachgewiesen, dass Paclitaxel durch den endophytisch lebenden Pilz Taxomyces andreanae biosynthetisiert wird. Endophyten sind Bakterien oder Pilze, welche in oder auf Pflanzen symbiotisch leben.
Entdeckung
Monroe E. Wall und M. C. Wani führten in den späten 1960er-Jahren gemeinsam eine umfassende Suche nach Anti-Krebs-Wirkstoffen durch. Dabei konnten sie im Jahre 1971 die Substanz Paclitaxel durch Extraktion der Rinde der Pazifischen Eibe (Taxus brevifolia) erstmals isolieren, charakterisieren und seine wucherungshemmende Wirkung auf Zellen, u. a. Krebszellen, feststellen.[4]
Pharmakologie
Anwendungsgebiete
Paclitaxel wird in der Therapie maligner Tumore (Chemotherapie) eingesetzt. Zu seinen Anwendungsgebieten gehören u. a. Ovarialkarzinome (in Kombination mit Cisplatin), Mammakarzinome (ggf. in Kombination mit Trastuzumab) und das nicht-kleinzellige Bronchialkarzinom (in Kombination mit Cisplatin oder Carboplatin) sowie das Prostatakarzinom (hier vor allem die synthetische Variante Docetaxel). Ferner wird es neben Sirolimus bei der Herzkatheterisierung (perkutante transluminale Koronarangioplastie, PTCA) zur Beschichtung von Stents („drug-eluting stents“) und Medikament-freisetzender Ballonkatheter (Drug-Eluting Ballons) verwendet, wodurch das Risiko eines erneuten Verschlusses der Koronararterie vermindert werden soll.
Wirkmechanismus
Paclitaxel wirkt, indem es die Teilung von Zellen (Mitose) stört. Es stört den Abbau von Mikrotubuli, die bei der Mitose Bestandteil der essenziellen Mitosespindel sind. Im Gegensatz zu Colchicin, Vinblastin und Nocodazol, die direkt den Aufbau der Mikrotubuli hemmen, inhibiert Paclitaxel deren Abbau.
Es wirkt somit auf alle sich teilenden Zellen, ist also nicht ohne Nebenwirkungen. Da Krebszellen sich schnell teilen, sind diese jedoch stärker betroffen.
Nebenwirkungen
Unter der Therapie mit Paclitaxel konnten folgende Nebenwirkungen beobachtet werden, die charakteristisch für die meisten Zytostatika sind: Knochenmarksuppression mit Blutbildveränderungen (Thrombozytopenie, Neutropenie, Anämie), Neuropathien (insbesondere Parästhesien), Myalgien, Haarausfall, gastrointestinale Nebenwirkungen (z. B. Übelkeit, Erbrechen, Durchfall).
Siehe auch
Literatur
- Eckhard Leistner (2005): Die Biologie der Taxane. In: Pharmazie in unserer Zeit. Bd. 34, S. 98–103. doi:10.1002/pauz.200400108
- Hans-Peter Lipp & Carsten Bokemeyer (2005): Therapie solider Tumoren: Wirksamkeit und Toxizität der Taxane. In: Pharmazie in unserer Zeit. Bd. 34, S. 128–137. doi:10.1002/pauz.200400113
Einzelnachweise
- ↑ a b Sicherheitsdatenblatt (Merck Biosciences)
- ↑ Liggins et al. (1997): Solid-state characterization of paclitaxel. In: J. Pham. Sci. Bd. 86, S. 1458-1463. PMID 9423162
- ↑ Paclitaxel bei ChemIDplus
- ↑ Wani, M. C.; Taylor, H. L.; Wall, M. E.; Coggon, P.; McPhail, A. T. J. Am. Chem. Soc. 1971, 93, 2325–2327.
Weblinks
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.
