- Tofranil
-
Strukturformel 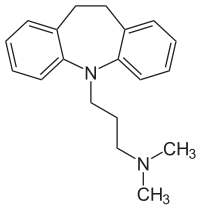
Allgemeines Freiname Imipramin Andere Namen 10,11-Dihydro-N,N-dimethyl-5H-dibenz- [b,f]azepin-5-propanamin (IUPAC)
Summenformel C19H24N2 CAS-Nummer - 50-49-7
- 113-52-0 (Imipramin-Hydrochlorid)
PubChem 3696 ATC-Code N06AA02
DrugBank APRD00672 Arzneistoffangaben Wirkstoffklasse Fertigpräparate Tofranil® (CH), Pryleugan® (D)
Verschreibungspflichtig: Ja Eigenschaften Molare Masse 280,40 g·mol−1 Schmelzpunkt 174,5 °C [1]
pKs-Wert 9,4 [1]
Löslichkeit Wasser: 18,2 mg·l−1 (24 °C) [1]
Sicherheitshinweise Gefahrstoffkennzeichnung [2]
Imipramin-Hydrochlorid
Xn
Gesundheits-
schädlichR- und S-Sätze R: 22-36/37/38 S: 26-36 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 WGK 3 (stark wassergefährdend) [2] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Imipramin zählt chemisch zur Klasse der Dibenzazepine und ist ein Arzneistoff aus der Gruppe der trizyklischen Antidepressiva.
Inhaltsverzeichnis
Geschichte
Imipramin war der erste moderne Arzneistoff zur Behandlung von Depressionen überhaupt und wurde zum Prototypen einer ganzen Klasse von Psychopharmaka. Entwickler und Hersteller war der Schweizer Konzern Geigy (heute Novartis); die Markteinführung erfolgte 1958.
Als Antidepressivum war es eine Zufallsentdeckung: Es sollte als Neuroleptikum bei Schizophreniekranken eingesetzt werden. Bei der klinischen Erprobung stellte man fest, dass es für diesen Zweck untauglich war, jedoch gegen depressive Symptome gut wirkte. Imipramin ist strukturell ein Analogon des Promazins (verbrückt mit –CH2–CH2– statt –S–).
Indikationen
Imipramin ist für die Therapie aller Formen von depressiven Erkrankungen zugelassen, bei Pavor nocturnus und Enuresis nocturna, außerdem zur adjuvanten Therapie chronischer Schmerzen.
Eine Anwendung bei Angstzuständen und Phobien ist gängig, geschieht allerdings ohne entsprechende Zulassung und damit Off-Label. Ebenso die Anwendung bei einer Retrograden Ejakulation.
Laut einer Studie von 2008 kommt es bei Patienten mit Panikstörungen, die Imipramin einnehmen und eine Kognitive Verhaltenstherapie (KVT) machen, häufiger zu Rückfällen als bei Patienten, die nur eine KVT machen.[3]
Imipramin wird auch bei Narkolepsie zur Therapie von Kataplexien eingesetzt.[4]
Wirkung
Imipramin hemmt im ZNS die Rückaufnahme von Monoaminen aus dem synaptischen Spalt in die präsynaptischen Vesikel und bewirkt so einen Konzentrationsanstieg der Neurotransmitter Serotonin und Noradrenalin im Plasma. Der bei Depressionen beobachtbare relative Mangel dieser Botenstoffe wird nun durch die erhöhte Verfügbarkeit ausgeglichen. Die so verbesserte neuronale Übertragung führt letztlich zu einer Milderung depressiver Symptome.
Imipramin greift in weitere Übertragungsprozesse im Gehirn ein und wirkt z. B. anticholinerg (als Antagonist bestimmter Acetylcholin-Wirkungen) und antihistaminisch. Es entstehen so die charakteristischen Nebenwirkungen der trizyklischen Antidepressiva.
Die aktivierenden und dämpfenden Teilwirkungen halten sich in etwa die Waage. Stimmungsaufhellende Stoffe mit einer ähnlich antriebsneutralen Wirkung werden auch als Antidepressiva vom Imipramin-Typ bezeichnet – mitunter selbst solche, die nicht zu den Trizyklika gehören.
Die sedierende Wirkkomponente vermindert sich meistens im Laufe der Anwendungsdauer; der stimmungsaufhellende Effekt tritt ebenfalls erst nach einer Einnahmedauer von circa 2–3 Wochen ein.
Darreichungsformen
Imipramin existiert als Generikum und als Originalpräparat (u.a. Tofranil®) in Form von Tabletten oder Dragees zur oralen Einnahme.
Schwangerschaft und Stillzeit
Es gibt klare Hinweise für Risiken des menschlichen Foetus, aber der therapeutische Nutzen für die Mutter kann überwiegen. Neugeborene, deren Mütter bis zur Geburt Imipramin eingenommen hatten, zeigten in den ersten Stunden oder Tagen Symptome wie Atemstörungen, Lethargie, Koliken, Reizbarkeit, Hypotonie, Hypertonie, Zittern oder Krämpfe. Zur Vermeidung dieser Symptome sollte Imipramin – soweit vertretbar – mindestens 7 Wochen vor dem errechneten Geburtstermin abgesetzt werden. Imipramin und sein Metabolit Desmethylimipramin treten in kleinen Mengen in die Muttermilch über. Da über die klinische Relevanz für den Säugling nichts bekannt ist, sollte abgestillt oder das Medikament abgesetzt werden.[5]
Reaktionsbereitschaft
Es können verschwommenes Sehen, Schläfrigkeit oder andere zentralnervöse Symptome auftreten. In diesem Fall sollten die Patienten kein Motorfahrzeug lenken, keine Maschinen bedienen und keine Tätigkeiten verrichten, die ihre volle Aufmerksamkeit erfordern.[5]
Unerwünschte Wirkungen
Imipramin hat vorwiegend vegetative Nebenwirkungen:
- Durstgefühl, Mundtrockenheit
- Hypotonie, Tachykardie, Herzrhythmusstörungen
- Mydriasis, Akkommodationsstörungen
- Obstipation, aber auch Diarrhoe u. a. Magen-Darm-Probleme
- Miktionsstörungen bis zum Harnverhalt
- Libidoverlust, Erektile Dysfunktion (Impotenz)
Weiterhin können auftreten:
- Schwindelgefühle, Kopfschmerzen
- Unruhe, Ataxie, Tremor
- Gewichtszunahme
- Hautausschlag
- Blutbildveränderungen, z. B. Leukopenie oder Agranulozytose
- Erregungsleitungsstörungen am Herzen.
Psychische Störwirkungen sind Müdigkeit, aber auch aggressives Verhalten und Verwirrtheit (selten: pharmakogenes Delir). Imipramin kann bei Bipolaren Erkrankungen ein Umschlagen einer depressiven in eine manische Phase bewirken.
Genotoxisches Potential
Im Tierversuch führte Imipramin zu Erbgutschäden. Möglicherweise erhöht die Einnahme von Imipramin das Brustkrebsrisiko.[6] [7]
Einzelnachweise
- ↑ a b c d e Imipramin bei ChemIDplus
- ↑ a b Datenblatt für Imipramine hydrochloride – Sigma-Aldrich 14. Januar 2008
- ↑ Raffa SD, Stoddard JA, White KS et al. Relapse following combined treatment discontinuation in a placebo-controlled trial for panic disorder. J Nerv Ment Dis. 2008 Jul;196(7):548–555. PMID 18626295.
- ↑ http://www.psychosoziale-gesundheit.net/psychiatrie/narkolepsie.html
- ↑ a b Fachinformation des Arzneimittel-Kompendium der Schweiz: Tofranil; Stand: Juni 1996.
- ↑ Pressemitteilung: Heavy exposure to some tricyclic antidepressants associated with elevated risk of breast cancer
- ↑ Sharpe CR, Collet JP, Belzile E et al. The effects of tricyclic antidepressants on breast cancer risk. Br J Cancer. 2002 Jan 7;86(1):92-7. PMID 11857018.
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.
