- 1-Fluor-2,4-dinitrobenzol
-
Strukturformel 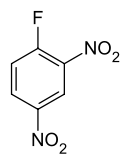
Allgemeines Name 1-Fluor-2,4-dinitrobenzol Andere Namen - Sangers Reagenz
- 2,4-Dinitro-1-fluorbenzol
- Dinitrofluorbenzol
- DNFB
Summenformel C6H3FN2O4 CAS-Nummer 70-34-8 PubChem 6264 Kurzbeschreibung gelbe Kristalle[1]
Eigenschaften Molare Masse 186,10 g·mol−1 Aggregatzustand fest
Dichte 1,482 g·cm−3 (25 °C)[2]
Schmelzpunkt Siedepunkt Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 

Achtung
H- und P-Sätze H: 302-315-317-319-335-373 EUH: keine EUH-Sätze P: 261-280-305+351+338 [2] EU-Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-33-36/37/38-43 S: 26-36/37 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. 1-Fluor-2,4-dinitrobenzol oder Sangers Reagenz ist ein gelber kristalliner Feststoff, die für die Proteinsequenzierung verwendet wird. Die Struktur besteht aus einem Benzolring mit einem Fluor (–F) und zwei Nitrogruppen (–NO2) als Substituenten. Es gehört zu einer Stoffgruppe, bei der sich durch unterschiedliche Anordnung der Substituenten sechs Konstitutionsisomere ergeben.
Inhaltsverzeichnis
Geschichte und Darstellung
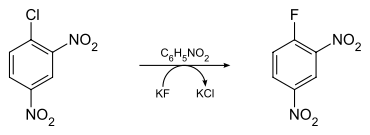
1-Fluor-2,4-dinitrobenzol wurde erstmals durch Holleman und Beekman im Jahr 1904 dargestellt. Sie erhielten es durch Nitrierung von p-Fluornitrobenzol, welches sie zuvor aus p-Nitroanilin dargestellt hatten.[4] Im Jahr 1936 stellte Gottlieb eine Synthese vor, bei der 1-Chlor-2,4-dinitrobenzol in Nitrobenzol mit Kaliumfluorid (KF) umgesetzt wurde.[5]
Deutliche Verbesserungen dieser Methode stellten Cook und Saunders im Jahr 1947 vor, die auf einer deutlichen Verringerung der Kaliumfluoridmenge und der Arbeitsschritte basierten. Sie erhitzten gleichfalls 1-Chlor-2,4-dinitrobenzol mit wasserfreiem Kaliumfluorid in Nitrobenzol bei 190–195 °C. Das Produkt wurde anschließend destillativ gereinigt. Bei einer Verwendung von Natriumfluorid (NaF) anstelle des Kaliumfluorids war dagegen praktisch keine Reaktion zu beobachten.[6]
Eigenschaften
1-Fluor-2,4-dinitrobenzol ist ein gelber kristalliner Feststoff, der bei 25,8 °C schmilzt und bei 296 °C siedet.[3] Es kristallisiert im orthorhombischen Kristallsystem in der Raumgruppe P2i2i2i mit den Gitterparametern a = 621,0 pm, b = 945 pm und c = 1285 pm und vier Formeleinheiten pro Elementarzelle.[7]
Verwendung
Im Jahr 1945 beschrieb Frederick Sanger die Verwendung von 1-Fluor-2,4-dinitrobenzol für die Bestimmung der N-terminalen Aminosäuren in Polypeptidketten, vor allem beim Insulin.[8] B. C. Saunders stellte ihm die Chemikalie freundlicherweise zur Verfügung, beide arbeiteten zu der Zeit an der Universität von Cambridge in England. Sangers erste Ergebnisse zeigten, dass Insulin ein kleineres Molekül war als bisher angenommen (molare Masse 12.000 g·mol−1), und dass sie aus vier Ketten bestehen (zwei enden mit Glycin und zwei enden mit Phenylalanin). Sanger setzte die Arbeit an Insulin mit Dinitrofluorbenzol in Kombination mit anderen Techniken fort, um schließlich die vollständige Sequenzierung des Insulins zu erreichen (bestehend aus nur zwei Ketten mit einer molaren Masse von 6000 g·mol−1).[9] Aufgrund dieser Arbeiten erhielt der Stoff die zusätzliche Bezeichnung Sangers Reagenz.
Nach der Erstveröffentlichung Sangers wurde die Dinitrofluorbenzol-Methode häufig für das Studium der Proteine angewendet, bis sie durch andere Reagenzien für die Terminal-Analyse abgelöst wurde (z. B. Dansylchlorid und später Aminopeptidasen und Carboxypeptidasen) sowie andere allgemeine Methoden zur Bestimmung der Sequenz (z. B. der Edman-Abbau).[9]
Einzelnachweise
- ↑ a b The Physical and Theoretical Chemistry Laboratory, Oxford University, Chemical and Other Safety Information: 2,4-dinitrofluorobenzene.
- ↑ a b c d Datenblatt 1-Fluoro-2,4-dinitrobenzene bei Sigma-Aldrich, abgerufen am 17. März 2011.
- ↑ a b c CRC Handbook of Chemistry and Physics, 90. Auflage, CRC Press, Boca Raton, Florida, 2009, ISBN 978-1-4200-9084-0, Section 3, Physical Constants of Organic Compounds, p. 3-260.
- ↑ A. F. Holleman, J. W. Beekman, in: Rec. Trav. chim. Pays-Bas, 1904, 23, S. 240.
- ↑ H. B. Gottlieb: The Replacement of Chlorine by Fluorine in Organic Compounds, in: J. Am. Chem. Soc., 1936, 58 (3), S. 532–533; doi:10.1021/ja01294a502.
- ↑ H. G. Cook, B. C. Saunders: 1:2:4-Fluorodinitrobenzene, in: Biochem. J., 1947, 41 (4), S. 558–559; PMID 20270792; PMC 1258537.
- ↑ A. Wilkins, R. W. H. Small: Structure of 1-Fluoro-2,4-dinitrobenzene, in: Acta Cryst., 1991, C47, S. 220–221; doi:10.1107/S0108270190007326.
- ↑ F. Sanger: The Free Amino Groups of Insulin, in: Biochem. J., 1945, 39 (5), S. 507–515; PMID 16747948; PMC 1258275.
- ↑ a b J. Fruton: Proteins, Enzymes, Genes: The Interplay of Chemistry and Biology. New Haven: Yale University Press, 1999, S. 216.
Literatur
- T. Schaefer: "The Proton Magnetic Resonance Spectrum of 1-Fluoro-2,4-dinitrobenzene", in: Canadian Journal of Chemistry, 1961, 40 (3), S. 431–433; doi:10.1139/v62-068.
- B. D. Nageswara Rao: "The 1H and 19F Resonance Spectra of 1-Fluoro-2,4-dinitrobenzene", in: Molecular Physics, 1964, 7 (4), S. 307–310; doi:10.1080/00268976300101071.
- Streitwieser / Heathcock: Organische Chemie, 1. Auflage, Verlag Chemie, Weinheim 1980, ISBN 3-527-25810-8, S. 996–997.
- Albert L. Lehninger: Biochemie, 2. Auflage, Verlag Chemie, Weinheim 1983, ISBN 3-527-25688-1, S. 82–83.
Weblinks
Kategorien:- Gesundheitsschädlicher Stoff
- Sensibilisierender Stoff
- Fluoraromat
- Nitrobenzol
Wikimedia Foundation.