- Germanium(IV)-fluorid
-
Strukturformel 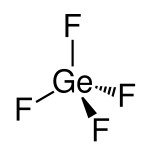
Allgemeines Name Germanium(IV)-fluorid Andere Namen - Germaniumtetrafluorid
- Tetrafluorgerman
Summenformel GeF4 CAS-Nummer 7783-58-6 PubChem 82215 Kurzbeschreibung farbloses Gas mit Knoblauch-artigem Geruch[1]
Eigenschaften Molare Masse 148,58 g·mol-1 Aggregatzustand gasförmig
Dichte 2,16 g·cm-3 (bei 0 °C)[1]
Schmelzpunkt Dampfdruck Löslichkeit Zersetzung in Wasser[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 
Gefahr
H- und P-Sätze H: 314 EUH: keine EUH-Sätze P: 280-305+351+338-310 [2] EU-Gefahrstoffkennzeichnung [1] 

Giftig Ätzend (T) (C) R- und S-Sätze R: 26-35 S: 9-26-28-36-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Germanium(IV)-fluorid ist eine chemische Verbindung aus der Gruppe der Germaniumverbindungen und Fluoride.
Inhaltsverzeichnis
Gewinnung und Darstellung
Germanium(IV)-fluorid lässt sich durch Reaktion von Germanium mit Fluor oder Fluorwasserstoff.[3]
Es entsteht auch bei der thermischen Zersetzung des Komplexsalzes Ba[GeF6], das durch Fällung einer Lösung von Germaniumdioxid in Flusssäure mit Bariumchlorid gewonnen werden kann.[3]
Eigenschaften
Germanium(IV)-fluorid ist ein nicht brennbares, an Luft stark rauchendes Gas mit knoblauchartigem Geruch. Es bildet mit Wasser ätzende Säuren (Hydrolyse zu GeO2 und H2GeF6) und kann mit diesen heftig reagieren. Oberhalb von 1000 °C zersetzt es sich, wobei Fluorwasserstoff, Fluor und Germaniumdioxid entstehen.[1][3] Aus wässrigen Lösungen kristallisiert es als Trihydrat aus.[4]
Verwendung
Germanium(IV)-fluorid wird in Kombination mit Disilan zur Herstellung von SiGe-Kristallen verwendet.[2]
Einzelnachweise
- ↑ a b c d e f g Eintrag zu CAS-Nr. 7783-58-6 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 19. Juni 2010 (JavaScript erforderlich)
- ↑ a b c Datenblatt Germanium(IV) fluoride bei Sigma-Aldrich, abgerufen am 3. April 2011.
- ↑ a b c Georg Brauer: Handbuch der Präparativen Anorganischen Chemie
- ↑ Holleman und Wiberg: Lehrbuch der anorganischen Chemie
Weblinks
GermaniumhalogenideGermanium(II)-fluorid | Germanium(II)-chlorid | Germanium(II)-bromid | Germanium(II)-iodid
Germanium(IV)-fluorid | Germanium(IV)-chlorid | Germanium(IV)-bromid | Germanium(IV)-iodid
Hexachlordigerman
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Germanium(IV)-chlorid — Strukturformel Allgemeines Name Germanium(IV) chlorid … Deutsch Wikipedia
Germaniumfluorid — steht für mehrere chemische Verbindungen von Germanium und Fluor: Germanium(II) fluorid, GeF2 Germanium(IV) fluorid, GeF4 Diese Seite ist eine Begriffsklärung zur Unterscheidung mehrerer mit demselben Wort bezeich … Deutsch Wikipedia
Chemikalienliste — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Liste chemischer Verbindungen — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Liste von chemischen Verbindungen — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Arsenvergiftung — Eigenschaften … Deutsch Wikipedia
Graues Arsen — Eigenschaften … Deutsch Wikipedia
Fluorchemie — Eigenschaften … Deutsch Wikipedia
Natururan — Eigenschaften … Deutsch Wikipedia
Uran-235 — Eigenschaften … Deutsch Wikipedia


