- Dichlordiphenyldichlorethan
-
Strukturformel 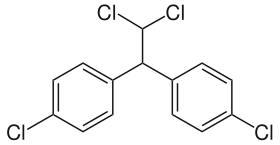
Allgemeines Name Dichlordiphenyldichlorethan Andere Namen - DDD
- p,p′-DDD
- TDE
- 1-Chlor-4-[2,2-dichlor-1-(4-chlorphenyl)ethyl]benzen (IUPAC)
Summenformel C14H10Cl4 CAS-Nummer 72-54-8 PubChem 6294 Eigenschaften Molare Masse 320,04 g·mol−1 Aggregatzustand fest
Dichte 1,476 g·cm−3 (20 °C) [1]
Schmelzpunkt 109,5 °C [2]
Siedepunkt 350 °C [2]
Dampfdruck Löslichkeit schlecht löslich in Wasser: 0,09 mg·l−1 (25 °C) [2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 


Gefahr
H- und P-Sätze H: 301-312-351-410 EUH: keine EUH-Sätze P: 273-280-301+310-501 [3] EU-Gefahrstoffkennzeichnung [1] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 21-25-40-50/53 S: 36/37-45-60-61 LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. p,p′-Dichlordiphenyldichlorethan (p,p′-DDD) ist eine chemische Verbindung. Es wurde als Insektizid verwendet und ist zudem auch ein Metabolit des verwandten Insektizids DDT.
 Reduktive Dechlorinierung von DDT zu DDD
Reduktive Dechlorinierung von DDT zu DDD
Inhaltsverzeichnis
Geschichte
In den 1940er- und 1950er-Jahren wurde p,p′-DDD zur Bekämpfung der Larven der Stechmückenart Clear Lake gnat im Wasser des Clear Lake in Kalifornien ausgebracht. Die Anwendungen führten jeweils nur zu einer Konzentration von einigen ppb p,p′-DDD im Seewasser und töteten rund 99 % der Mückenlarven im Seeschlamm. Das ausgebrachte p,p′-DDD reicherte sich durch Biomagnifikation jedoch über die Nahrungskette an und führte zum Zusammenbruch des Renntaucher-Bestands an diesem See. Im Plankton war die p,p′-DDD-Konzentration bereits rund 265 mal so hoch wie im Wasser, bei Raubfischen und Vögeln war sie etwa um den Faktor 85 000 erhöht. So enthielt analysiertes Körperfett verendeter Renntaucher rund 1600 ppm p,p′-DDD.[4]
Gewinnung und Darstellung
p,p′-DDD wurde durch Kondensation von Dichloracetaldehyd mit Chlorbenzol hergestellt.[5] In technischem DDT ist p,p′-DDD je nach Quelle mit 0,3 % oder < 4 % enthalten.[6]
Verwendung
p,p′-DDD wurde als Insektizid verwendet. Produktionszahlen sind nicht bekannt, es hatte jedoch keine große Bedeutung.[5]
Das isomere o,p′-DDD wird in der Veterinärmedizin unter dem Wirkstoffnamen Mitotan zur Behandlung des Cushing-Syndroms bei Hunden eingesetzt, verliert jedoch aufgrund seiner toxischen Eigenschaften gegenüber moderneren Medikamenten zunehmend an Bedeutung.
Einzelnachweise
- ↑ a b Eintrag zu 1,1-Dichlor-2,2-bis(4-chlorphenyl)ethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 27. Januar 2010 (JavaScript erforderlich)
- ↑ a b c d e Dichlordiphenyldichlorethan bei ChemIDplus
- ↑ a b Datenblatt 1,1-Dichloro-2,2-bis(4-chlorophenyl)ethane bei Sigma-Aldrich, abgerufen am 24. März 2011.
- ↑ Thomas R. Dunlap, DDT: Scientists, Citizens and Public Policy. Princeton University Press, 1981, ISBN 0-691-04680-8, S. 94–96
- ↑ a b U.S. Department of Health and Human Services, Agency for Toxic Substances and Disease Registry: Toxicological profile for DDT, DDE and DDD., 2002
- ↑ Beratergremium für Altstoffe der Gesellschaft Deutscher Chemiker: DDT und Derivate – Modellstoffe zur Beschreibung endokriner Wirkungen mit Relevanz für die Reproduktion. BUA-Stoffbericht 216, S. Hirzel Verlag, August 1998, ISBN 3-7776-0961-7
Weblinks
Kategorien:- Giftiger Stoff
- Gesundheitsschädlicher Stoff
- Stoff mit Verdacht auf krebserzeugende Wirkung
- Umweltgefährlicher Stoff
- Chloralkan
- Chloraromat
- Insektizid
- Biozid (Wirkstoff)
Wikimedia Foundation.
