- Hypochlorige Säure
-
Strukturformel 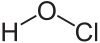
Allgemeines Name Hypochlorige Säure Andere Namen Unterchlorige Säure
Summenformel HClO CAS-Nummer 7790-92-3 PubChem 24341 Kurzbeschreibung schwach grüngelb gefärbte, chlorkalkartig riechende Substanz, die nur in wässriger Lösung beständig ist.[1]
Eigenschaften Molare Masse 52,46 g·mol−1 pKs-Wert 7,54[2]
Löslichkeit löslich in Wasser[1]
Sicherheitshinweise EU-Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Hypochlorige Säure (veraltet Unterchlorige Säure) HClO, ist eine farblose (konzentrierte Lösungen sind durch Dichloroxid schwach gelb gefärbt[2]), chlorkalkartig riechende, nur schwach dissoziierende Säure. Sie wirkt bleichend und oxidierend.
Inhaltsverzeichnis
Gewinnung und Darstellung
Sie wird durch Einleiten von Chlor in Wasser und gleichzeitiger Beseitigung der entstehenden Salzsäure durch Quecksilberoxid hergestellt[2].
Zuletzt kann chloridfreie Hypochlorige Säure durch Reaktion von Dichloroxid mit Wasser hergestellt werden.[4]
Eigenschaften
Die Säure ist unbeständig und nur in wässriger Lösung herstellbar. Selbst in geringen Konzentrationen neigt sie zur Disproportionierung zu Chlorsäure und Salzsäure.
Die Salze und Ester der Hypochlorigen Säure heißen Hypochlorite.
Verwendung
Desinfektion von Badewasser in Schwimmbädern, zum Beispiel bei der Langzeitchlorung mit Trichlorisocyanursäuretabletten (TCCS), welche langsam mit dem Beckenwasser zu Cyanursäure und Hypochloriger Säure reagieren. In seltenen Fällen wird Hypochlorige Säure auch zur Trinkwasseraufbereitung eingesetzt.
Sicherheitshinweise
Hypochlorige Säure ist zwar nur eine schwache Säure; sie kann allerdings durch ihre starke Oxidationswirkung dennoch Reizungen der Haut und sogar Verätzungen verursachen. Bei ihrem Zerfall entstehen stark ätzende Stoffe, wie Chlorsäure und Salzsäure, die organisches Gewebe innerhalb kürzester Zeit gänzlich abtöten oder sogar vollkommen zersetzen können. Zu beachten ist, dass Hypochlorige Säure niemals zur Oxidation von Alkoholen eingesetzt werden darf, da sie mit ihnen durch Veresterung hochexplosive Alkylhypochlorite bilden können. Mit Ammoniak bildet sich das explosive Stickstofftrichlorid[2].
Einzelnachweise
- ↑ a b Eintrag zu CAS-Nr. 7790-92-3 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 21. August 2007 (JavaScript erforderlich).
- ↑ a b c d Holleman/Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, Berlin 2007, ISBN 978-3-11-017770-1.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., Band 1, Academic Press 1963, S. 308-9.
ChlorsauerstoffsäurenHypochlorige Säure | Chlorige Säure | Chlorsäure | Perchlorsäure
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Unterchlorige Säure — Strukturformel Allgemeines Name Hypochlorige Säure Andere Namen Unterchlorige Säure … Deutsch Wikipedia
Chlorige Säure — Strukturformel Allgemeines Name Chlorige Säure Andere Namen … Deutsch Wikipedia
HOCl — Strukturformel Allgemeines Name Hypochlorige Säure Andere Namen Unterchlorige Säure … Deutsch Wikipedia
Liste mit Säuren — Die folgende Liste zeigt eine Auswahl von Säuren. Aufgelistet sind der gebräuchliche Trivialname der IUPAC Name (die offizielle Bezeichnung) die Summenformel oder eine vereinfachte Strukturformel Die Liste erhebt keinen Anspruch auf… … Deutsch Wikipedia
Sauerstoffsäure — Die folgende Liste zeigt eine Auswahl von Säuren. Aufgelistet sind der gebräuchliche Trivialname der IUPAC Name (die offizielle Bezeichnung) die Summenformel oder eine vereinfachte Strukturformel Die Liste erhebt keinen Anspruch auf… … Deutsch Wikipedia
Chlorbleiche — Chlorwasser nennt man die Lösung von Chlorgas in Wasser. Herstellung und Chemie In Wasser ist Chlor gut löslich. In einem Liter Wasser löst sich 0,0921 mol Chlor (25°C,101325 Pa)[1]. Auf Grund der Disproportionierung des Chlors bildet sich neben… … Deutsch Wikipedia
Chlorwasser — nennt man die Lösung von Chlorgas in Wasser. Herstellung und Chemie In Wasser ist Chlor gut löslich. In einem Liter Wasser löst sich 0,0921 mol Chlor (25°C,101325 Pa)[1]. Auf Grund der Disproportionierung des Chlors bildet sich neben… … Deutsch Wikipedia
Chlorsäure — Strukturformel Allgemeines Name Chlorsäure Andere Namen C … Deutsch Wikipedia
HClO3 — Strukturformel Allgemeines Name Chlorsäure Andere Namen Chlor(V) säure … Deutsch Wikipedia
Chlorchemie — Eigenschaften … Deutsch Wikipedia

