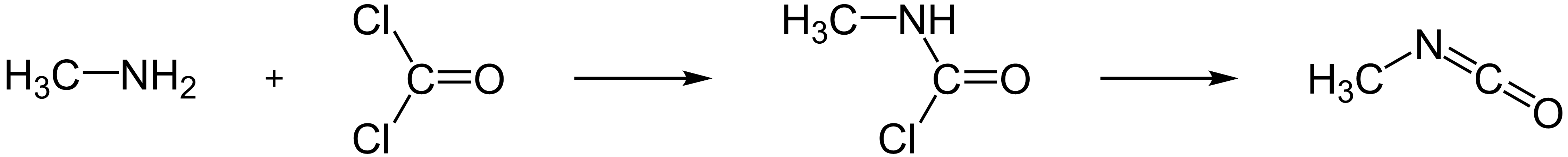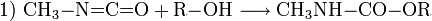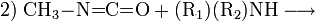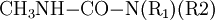- Isocyansäuremethylester
-
Strukturformel 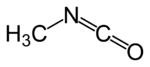
Allgemeines Name Methylisocyanat Andere Namen - MIC
- Isocyanatomethan
- Isocyansäuremethylester
Summenformel CH3NCO CAS-Nummer 624-83-9 Kurzbeschreibung flüchtige, farblose Flüssigkeit Eigenschaften Molare Masse 57,1 g·mol−1 Aggregatzustand flüssig
Dichte Schmelzpunkt Siedepunkt 38 °C [1]
Dampfdruck 46,4 kPa (20 °C)[1]
Löslichkeit zersetzt sich in Wasser
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Leicht-
entzündlichSehr giftig (F) (T+) R- und S-Sätze R: 11-24/25-26-37/38-41-42/43-63 S: (1/2)-16-26-27/28-36/37/39-45-63 MAK 0,024 mg·m−3[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Methylisocyanat (kurz MIC) ist der einfachste Ester der Isocyansäure. Es ist eine sehr reaktive chemische Verbindung, die z. B. bei der Herstellung von Insektiziden verwendet wird. Wie die Isocyansäure und die anderen Isocyanate ist es sehr giftig.
Inhaltsverzeichnis
Geschichte
Im indischen Bhopal ereignete sich am 3. Dezember 1984 ein schwerer Chemieunfall mit Methylisocyanat (Katastrophe von Bhopal). Dabei entwichen aus einem defekten Tank einer Pestizidfabrik des amerikanischen Chemiekonzerns Union Carbide Corporation in der Nähe der Stadt über 40 Tonnen Methylisocyanat. Bei diesem Chemieunfall kamen tausende Menschen ums Leben. Zudem kam es zu einer immensen Verseuchung der Umwelt.
Gewinnung und Darstellung
Technisch wird Methylisocyanat durch Reaktion von Methylamin und Phosgen hergestellt. Nach Abspaltung von Chlorwasserstoff (HCl) wird das Zwischenprodukt N-Methylcarbamoylchlorid in Methylisocyanat umgewandelt:
Methylamin reagiert im ersten Schritt bei −20 °C bis 60 °C mit Phosgen unter HCl-Abspaltung zu N-Methylcarbamoylchlorid. Im zweiten Schritt bei 100–200 °C entsteht unter erneuter Eliminierung von HCl Methylisocyanat.
Eigenschaften
Methylisocyanat ist eine flüchtige, farblose Flüssigkeit, die stark tränenerregend ist und konzentriert einen stechenden Geruch aufweist. Sie ist leicht entflammbar (Flammpunkt bei −7 °C). Bei leicht erhöhten Temperaturen (38 °C) geht sie in den gasförmigen Aggregatzustand über, in welchem sie schwerer als Luft ist und mit dieser leicht explosive Gemische bildet (Explosionsgrenzen: 5,3–26 Volumenprozent Methylisocyanat). Gasförmiges Methylisocyanat entzündet sich selbstständig bei 535 °C.
Verwendung
Methylisocyanat wird vor allem zur Herstellung von Carbamaten durch Umsetzung mit einem Alkohol (1) oder zur Herstellung von speziellen Harnstoffen durch Umsetzung mit Aminen (2) verwendet:
In der Pestizidfabrik des amerikanischen Chemiekonzerns Union Carbide Corporation in der Nähe der Stadt Bhopal wurden seinerzeit die Wirkstoffe Carbaryl (CAS Nr. 63-25-2) und Aldicarb (2-Methyl-2-(methylthio)propionaldehyd-O-methylcarbamoyloxim, CAS Nr. 116-06-3) produziert.
Physiologie
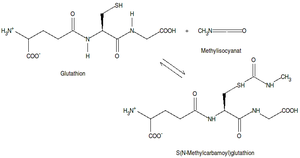
Die direkte Toxizität von Methylisocyanat resultiert aus der Fähigkeit, zahlreiche nukleophile Gruppen stoffwechselaktiver Biomoleküle anzugreifen. Der Mechanismus für den Transport wurde 1992 entdeckt. Demnach kann Glutathion, ein Tripeptid, dessen Aufgabe es eigentlich ist, den Organismus vor der Schädigung durch toxische Substanzen zu schützen, Methylisocyanat reversibel an die Thiolgruppe addieren und damit im Körper transportieren.
Sicherheitshinweise
Methylisocyanat verursacht bei Exposition Verätzungen der Schleimhäute, Augen und Lungen, jedoch wurden bei Opfern des Bhopalunglücks vielfach auch schwere Verätzungen innerer Organe festgestellt. Dieser Befund war insofern überraschend, als Methylisocyanat zu reaktiv ist, um unverändert in den Kreislauf zu gelangen.
Methylisocyanat ist möglicherweise fruchtschädigend.
Quellen
- ↑ a b c d e Eintrag zu Methylisocyanat in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 25.4.2008 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 624-83-9 im European chemical Substances Information System ESIS
Weblinks
Wikimedia Foundation.