- Mangan(II)-nitrat
-
Strukturformel 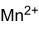
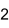
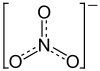
Allgemeines Name Mangan(II)-nitrat Summenformel MnN2O6 CAS-Nummer - 10377-66-9
- 15710-66-4 Hydrat
- 20694-39-7 Tetrahydrat
- 17141-63-8 Hexahydrat
Kurzbeschreibung blaßrosafarbener Feststoff [1]
Eigenschaften Molare Masse 178,94 g·mol−1 Aggregatzustand fest
Dichte 2,13 g·cm−3[1]
Schmelzpunkt Siedepunkt Löslichkeit sehr gut in Wasser (3800 g·l−1 bei 20 °C) [1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 



Gefahr
H- und P-Sätze H: 272-302-314-373-412 EUH: 071 P: 220-261-305+351+338 (Tetrahydrat)[2] EU-Gefahrstoffkennzeichnung [1] 
Brand-
fördernd(O) R- und S-Sätze R: 8-22-34-48/20-52/53 S: keine S-Sätze MAK 0,5 mg·m−3[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Mangan(II)-nitrat ist das Nitratsalz des Mangans mit der Summenformel Mn(NO3)2.
Inhaltsverzeichnis
Gewinnung und Darstellung
Mangan(II)-nitrat kann durch Lösung von Mangan(II)-carbonat in verdünnter Salpetersäure:
Ebenfalls möglich ist die Herstellung durch Reaktion Mangan(IV)-oxid und Stickstoffdioxid.[3]
Eigenschaften
Mangan(II)-nitrat ist ein blassrosafarbener Feststoff, welcher sehr gut löslich in Wasser ist. Er zersetzt sich ab einer Temperatur 140 °C.[1] Mangan liegt hier in der Oxidationsstufe +2 vor. Das Salz bildet je nach Herstellungsmethode und Temperatur ein Monohydrat, ein Trihydrat oder ein Hexahydrat.[4] Es ist wie viele andere Nitrate ein Oxidationsmittel und wirkt brandfördernd.
Verwendung
Mangan(II)-nitrat wird zur Herstellung von hochreinen Manganoxiden, Spinellen und Porzellanfarben verwendet.[1] Zudem wird es im Getreideanbau als Blattdünger zur Förderung der Wurzelbildung eingesetzt.[5]
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu CAS-Nr. 10377-66-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 17. September 2011 (JavaScript erforderlich)
- ↑ Datenblatt Manganese(II) nitrate tetrahydrate, purum p.a., ≥97.0% (KT) bei Sigma-Aldrich, abgerufen am 17. September 2011.
- ↑ Arno H. Reidies, “Manganese Compounds” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a16_123
- ↑ ABC Chemie, Verlag Harri Deutsch Frankfurt/Main und Zürich 1965
- ↑ agrarservice.de
Wikimedia Foundation.

