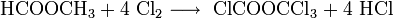- Methansäuremethylester
-
Strukturformel 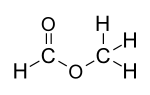
Allgemeines Name Ameisensäuremethylester Andere Namen - Methylformiat
- Methansäuremethylester
- Methylmethanat
Summenformel C2H4O2 CAS-Nummer 107-31-3 [1] Kurzbeschreibung farblose, sehr leicht flüchtige Flüssigkeit mit geringer Oberflächenspannung Eigenschaften Molare Masse 60,05 g/mol [1] Aggregatzustand flüssig
Dichte 0,97 g·cm–3 [1]
Schmelzpunkt Siedepunkt 31–33 °C [1]
Dampfdruck Löslichkeit gut in Alkohol, Aceton, Ether
mäßig löslich in Wasser (300 g/l) [1]Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Hoch-
entzündlichGesundheits-
schädlich(F+) (Xn) R- und S-Sätze R: 12-20/22-36/37 S: (2)-9-16-24-26-33 MAK 120 mg·m–3 [3]
LD50 1500 mg/kg [1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Ameisensäuremethylester (auch Methylformiat oder Methansäuremethylester) ist eine chemische Verbindung mit der Summenformel C2H4O2 und der molaren Masse von 60,05 g/mol. Es ist der Methylester der Ameisensäure, also der einfachste Vertreter dieser Stoffgruppe.
Inhaltsverzeichnis
Eigenschaften
Ameisensäuremethylester ist eine farblose, sehr leicht flüchtige Flüssigkeit mit angenehmem Geruch, die Geruchsschwelle liegt bei 500 bis 68750 mg/m3. Sie zeigt eine ziemlich kleine Oberflächenspannung.
Mit Wasser ist der Ester in begrenztem Umfang mischbar (~1:3), wobei sich diese Mischungen vergleichsweise schnell in umgekehrter Bildungsreaktion zu Methanol und Ameisensäure zersetzen.
Der MAK-Wert liegt bei 100 ml/m3, die CAS-Nummer lautet 107-31-3. Ameisensäuremethylester ist hochentzündlich, der Flammpunkt liegt nach DIN 51755 bei -28 °C, und ein schwach wassergefährdender Stoff.
Herstellung
Setzt man Methanol im stark alkalischen mit Kohlenstoffmonoxid um, so entsteht in einer Additionsreaktion Ameisensäuremethylester:
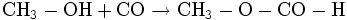
Auch die Reaktion von Methanol mit Ameisensäure kann zur Herstellung kleinerer Mengen genutzt werden, jedoch nur mit begrenzter Ausbeute:
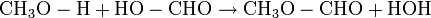 Aufgrund der im Vergleich zu anderen Carbonsäuren leichten Dehydratisierbarkeit der Ameisensäure können hierbei allerdings keine starken Trockenmittel wie z. B. konz. Schwefelsäure verwendet werden.
Aufgrund der im Vergleich zu anderen Carbonsäuren leichten Dehydratisierbarkeit der Ameisensäure können hierbei allerdings keine starken Trockenmittel wie z. B. konz. Schwefelsäure verwendet werden.Verwendung
Ameisensäuremethylester wird als Lösungsmittel für diverse Natur- und Kunstharze verwendet, da es aufgrund seiner großen Flüchtigkeit diese sehr schnell trocknen lässt. Es dient auch als Insektizid und als Kältemittel (R611).
Es ist weiterhin von Bedeutung bei der Synthese von Ameisensäure:
- Aus den billigen chemischen Grundstoffen Methanol und Kohlenstoffmonoxid wird Ameisensäuremethylester hergestellt.
- Durch Versetzen mit Wasser unter energischen Bedingungen wird der Ester leicht quantitativ zu Methanol und Ameisensäure hydrolysiert („verseift“). Da Methanol unterm Strich als Edukt und als Produkt vorkommt, wirkt es quasi als Katalysator der Wasseranlagerung an CO. Außerdem dient Methylformiat zur Herstellung von Formamid, Dimethylformamid und verschiedener Medikamente. Statt Wasser kann man es - aufgrund der günstigen Siedetemperatur und der niedrigeren Verdampfungswärme - in Solarkollektoren einsetzen, um diese wirtschaftlicher zur Stromerzeugung zu nutzen.
Man kann aus Ameisensäuremethylester auch Diphosgen herstellen, in dem man es unter UV-Licht chloriert:
Quellen
- ↑ a b c d e f g h Sicherheitsdatenblatt (Merck)
- ↑ Eintrag zu CAS-Nr. 107-31-3 im European chemical Substances Information System ESIS
- ↑ Eintrag zu CAS-Nr. 107-31-3 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 30. März 2008 (JavaScript erforderlich)
Wikimedia Foundation.