- Dimethylformamid
-
Strukturformel 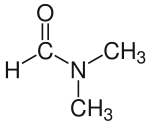
Allgemeines Name Dimethylformamid Andere Namen - N,N-Dimethylmethanamid
- N,N-Dimethylformamid
- Ameisensäuredimethylamid
- DMF
Summenformel C3H7NO CAS-Nummer 68-12-2 Kurzbeschreibung Eigenschaften Molare Masse 73,10 g·mol−1 Aggregatzustand flüssig
Dichte 0,95 g·cm−3 (20 °C)[1]
Schmelzpunkt Siedepunkt 153 °C[1]
Dampfdruck Löslichkeit mischbar mit Wasser und vielen organischen Lösungsmitteln[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 


Gefahr
H- und P-Sätze H: 360D-226-332-312-319 EUH: keine EUH-Sätze P: 201-302+352-305+351+338-308+313 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 
Giftig (T) R- und S-Sätze R: 61-20/21-36 S: 53-45 MAK 15 mg·m−3[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Dimethylformamid (DMF), genauer N,N-Dimethylformamid ist ein Amid der Ameisensäure. DMF wird als polares, organisches Lösungsmittel eingesetzt.
Inhaltsverzeichnis
Herstellung
Die großtechnische Herstellung von DMF erfolgt auf zwei verschiedenen Wegen, nach einem einstufigen und einem zweistufigen Prozess. Bei der einstufigen Synthese wird Dimethylamin mit Kohlenmonoxid bei erhöhter Temperatur und erhöhtem Druck direkt zu DMF umgesetzt. Die Reaktion wird in der Flüssigphase mit Hilfe eines Katalysators (Natriumethylat) durchgeführt:
Bei der zweistufigen Synthese wird die Umsetzung von Dimethylamin mit Ameisensäuremethylester durchgeführt, es entsteht Methanol als Nebenprodukt:
Beide Synthesen verlaufen mit hohen Ausbeuten ohne die Bildung nennenswerter Nebenprodukte. Die Produktaufarbeitung erfolgt in beiden Fällen durch mehrstufige Destillation.
Verwendung
- DMF dient als Lösungsmittel für eine Vielzahl von festen, flüssigen oder gasförmigen Stoffen, für Polymere, wie beispielsweise Polyacrylnitril, PVC, Polyamide, Polyurethane, Epoxidharze, sowie für Cellulose und deren Derivate.
- DMF wird im Labor, da polar aprotisch, bei Reaktionen mit polaren Übergangszuständen gerne als Lösemittel verwendet. Bei nukleophilen Substitutionen können gegenüber z.B. Methanol drastische Geschwindigkeitserhöhungen verzeichnet werden.
- DMF dient in der chemischen Technik als Extraktionsmittel zur Abtrennung von Benzol, Ethin, 1,3-Butadien.
- DMF ist ein Zusatzstoff zu Flugbenzin, es dient als Katalysator für dessen Verbrennung
- DMF ist ein Zwischenprodukt in der Synthese von Acetalen, Aldehyden, Carbonsäureestern und Nitrilen
- Aus DMF und Phosphoroxychlorid lässt sich das Vilsmeier-Haack-Reagenz, das zur Formylierung von Aromaten und zur Chlorierung von Carbonsäuren dient, herstellen.
- DMF zersetzt sich unter Licht und Hitzeeinwirkung zu Dimethylamin und Formaldehyd, so dass diese Substanzen, die normalerweise als wässrige Lösung erhältlich sind, in situ wasserfrei erzeugt werden können.[4]
Sicherheitshinweise
Sowohl nach akuter als auch nach chronischer Einwirkung kommt es zu einer Leberzellschädigung. Histologisch zeigen sich mikrovesikuläre Fetteinlagerungen (Fettleber) und Veränderungen des Lebergewebes ohne ausgeprägte Entzündungen.
Der Stoff ist in Anlage 6 zu Nummer 30 des Anhangs XVII der REACh-Verordnung (EG) Nr. 1907/2006 als fortpflanzungsgefährdend der Kategorie 2 gelistet.
Einzelnachweise
- ↑ a b c d e f g Eintrag zu Dimethylformamid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 28.4.2008 (JavaScript erforderlich)
- ↑ a b Roempp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b Eintrag zu CAS-Nr. 68-12-2 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Trocknung von N,N-Dimethylformamid mit Phosphor(V)-oxid. Betriebsanweisung des Institut für Organische Chemie an der Universität Würzburg.
Kategorien:- Stoff mit reproduktionstoxischer Wirkung
- Gesundheitsschädlicher Stoff
- Formamid
Wikimedia Foundation.


