- 3-Aminobenzoesäure
-
Strukturformel 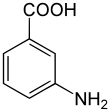
Allgemeines Name 3-Aminobenzoesäure Andere Namen - m-Aminobenzoesäure
- meta-Aminobenzoesäure
- m-Anthranilsäure
- 3-Carboxyanilin
Summenformel C7H7NO2 CAS-Nummer 99-05-8 PubChem 7419 Kurzbeschreibung weißes kristallines nahezu geruchloses Pulver[1]
Eigenschaften Molare Masse 137,14 g·mol−1 Aggregatzustand fest
Dichte 1,51 g·cm−3[1]
Schmelzpunkt pKs-Wert 3,07[2]
Löslichkeit schlecht in Wasser (5,9 g·l−1 bei 20 °C)[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 302-315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [3] EU-Gefahrstoffkennzeichnung [3] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/37/38 S: 26 LD50 6300 mg·kg−1 (Maus, oral)[3]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. 3-Aminobenzoesäure ist eine organische Carbonsäure, die zur Herstellung von Azofarbstoffen verwendet wird. Neben der 3-Aminobenzoesäure existieren zwei weitere stellungsisomere Formen: die Anthranilsäure (o-Aminobenzoesäure) und die 4-Aminobenzoesäure (p-Aminobenzoesäure).
Gewinnung und Darstellung
3-Aminobenzoesäure kann durch die Reduktion von 3-Nitrobenzoesäure erhalten werden. Als Reduktionsmittel eignen sich beispielsweise elementares Zink in Salzsäure[4] oder Hydrazin[5].
Toxikologie
3-Aminobenzoesäure zeigt geringe Toxizität. Außerdem wurden keine Hinweise auf Reproduktionstoxizität, Mutagenität und Kanzerogenität gefunden.[1]
Einzelnachweise
- ↑ a b c d e Eintrag zu 3-Aminobenzoesäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. November 2008 (JavaScript erforderlich).
- ↑ CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ a b c d Datenblatt 3-Aminobenzoesäure bei Sigma-Aldrich, abgerufen am 8. November 2008.
- ↑ J. Wilbrand, F. K. Beilstein: Ueber eine neue Reihe isomerer Verbindungen der Benzoëgruppe. – Nitrodracylsäure und deren Derivate, in: J. Liebigs Ann. Chem., 1863, 128, S. 257–273; doi:10.1002/jlac.18631280302.
- ↑ T. Curtius: Die Einwirkung von Hydrazinhydrat auf Nitroverbindungen. I. Abhandlung, in: J. Prakt. Chem., 1907, 76, S. 233–237; doi:10.1002/prac.19070760116.
Wikimedia Foundation.
