- Retinol
-
Strukturformel 
Allgemeines Trivialname Vitamin A1 Andere Namen - Retinol
- Axerophthol
- (2E,4E,6E,8E)-3,7-Dimethyl- 9-(2,6,6-trimethylcyclohex-1-enyl)nona- 2,4,6,8-tetraen-1-ol (IUPAC)
Summenformel C20H30O CAS-Nummer 68-26-8 ATC-Code Kurzbeschreibung gelber Feststoff Vorkommen z. B. in Fisch, Leber, Eigelb, Milch Physiologie Funktion Bestandteil des Sehpigments, Wachstumsfaktor, beteiligt bei Testosteronbildung Täglicher Bedarf 0,8–1,0 mg Folgen bei Mangel u. a. Haarausfall, Sehstörungen (z. B. Nachtblindheit), Atrophie von Schleimhäuten und Speicheldrüsen Überdosis 7,5 mg Eigenschaften Molare Masse 286,46 g·mol−1 Aggregatzustand fest Schmelzpunkt 61–63 °C [1] Siedepunkt 120–125 °C [1] Löslichkeit praktisch unlöslich in Wasser [1], gut in unpolaren Lösungsmitteln Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 
Achtung
H- und P-Sätze H: 302-315 EUH: keine EUH-Sätze P: keine P-Sätze [2] Gefahrstoffkennzeichnung [2] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/38-63 S: 26-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Retinol, auch Vitamin A1 oder Axerophthol, ist ein fettlösliches, essenzielles Vitamin. Chemisch gesehen gehört Retinol zu den Diterpenen und ist ein einwertiger, primärer Alkohol. Der enthaltene Ring aus sechs Kohlenstoffatomen wird β-Jononring genannt, und das Molekül weist zudem eine Reihe konjugierter Doppelbindungen auf, die für seine Beteiligung am Sehvorgang entscheidend sind.
Oftmals wird, auch in vielen Lehrbüchern, Retinol vereinfachend mit Vitamin A gleichgesetzt. Man versteht jedoch unter Vitamin A vielmehr eine Stoffgruppe von β-Jononderivaten, die dasselbe biologische Wirkungsspektrum wie all-trans-Retinol aufweisen, ausschließlich der Provitamine A.[3]
Inhaltsverzeichnis
Geschichte
Retinol wurde 1913 von Elmer McCollum und Marguerite Davis entdeckt.[4] Sie beschrieben es als ein fettlösliches Vitamin und dessen Bedeutung als antixerophthalmatischen Faktor. Erst 20 Jahre später erfolgte die Reindarstellung des Retinols aus Lebertran durch Paul Karrer.
Die erste Totalsynthese von Retinol gelang 1947 den holländischen Chemikern Jozef Ferdinand Arens und David Adriaan van Dorp durch schrittweise Reduktion von Tretinoin. Nach ihnen wurde diese Synthese Arens-van Dorp-Synthese genannt.[5]
Vorkommen
Natürliche Retinolquellen sind Fisch, Leberprodukte, Butter, Eigelb und Milchprodukte.
Stoffwechsel
Der Vitamin-A-Stoffwechsel wird im Wesentlichen durch sogenannte RBPs (Retinol-Bindeproteine) gesteuert. Nur mit deren Hilfe wird Vitamin A für den Körper nutzbar, wodurch ein Mangel an diesen Proteinen zu ähnlichen Symptomen führen kann wie ein Vitamin-A-Mangel (Hypovitaminose) selbst.
Kann überschüssiges Retinol nicht durch RBPs gebunden werden, so treten Vergiftungserscheinungen auf. Sie spielen daher auch bei einer Hypervitaminose A eine entscheidende Rolle. Da sie einen sogenannten Zinkfinger besitzen, ist das Spurenelement Zink wichtig für den gesamten Vitamin-A-Haushalt – sowohl bei Unter- als auch Überversorgung.
Reaktionen
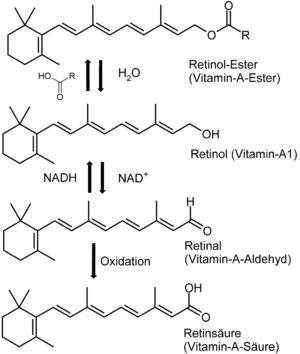
Die Synthese Vitamin-A-aktiver Verbindungen geht von einem Retinol-Ester (meist Vitamin-A-Palmitat) aus:
Bedarf
Der Mensch benötigt Vitamin A1 (Retinol), kann aber auch Provitamin A (β-Carotin) nutzen. Da das Provitamin nicht gleichermaßen utilisierbar ist (Resorption, Umwandlung) ist sein Bedarf höher. Grob wird von der Deutschen Gesellschaft für Ernährung (DGE) der Bedarf für den Erwachsenen folgendermaßen angegeben:
- 1 mg Vitamin A
- 2 mg β-Carotin
- 0,5 mg Vitamin A und 1 mg β-Carotin.
Die Katze benötigt ebenfalls Retinol oder Vitamin A1, nimmt aber eine Sonderstellung ein, da sie im Gegensatz zu fast allen anderen Tieren nicht β-Carotin in Retinol umwandeln kann und sich daher natürlicherweise nur durch den Genuss von Leber mit Vitamin A ausreichend versorgen kann.[6]
Synthese
Ein Schlüsselschritt bei der großtechnischen Herstellung von Vitamin A ist die Wittig-Reaktion. Für diese weithin anwendbare Reaktion erhielt Georg Wittig im Jahre 1979 den Nobelpreis für Chemie.
Im ersten Teil der Synthese wird von Dehydrolinalool aus ein C15-Salz hergestellt. Dieses reagiert durch die Wittig-Reaktion mit einem C5-Acetat, das aus Dimethoxyaceton hergestellt wird, zum Retinolacetat. Dieses kann über mehrere weitere Schritte in das Retinol umgewandelt werden.
1 RE (Retinol-Äquivalent) = 1 Mikrogramm Retinol = 6 Mikrogramm β-Carotin
Einzelnachweise
- ↑ a b c d Eintrag zu Retinol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Dezember 2007 (JavaScript erforderlich).
- ↑ a b Datenblatt Retinol bei Sigma-Aldrich, abgerufen am 22. April 2011.
- ↑ Hanck, Kuenzle, Rehm: Vitamin A. Blackwell Wissensch., Berlin, 1991 ISBN 978-3-8263-2879-4.
- ↑ McCollum & Davis (1913): The necessity of certain lipids during growth. In: J. Biol. Chem. Bd. 15, S. 167–175.
- ↑ Jozef Ferdinand Arens, David Adriaan van Dorp: Synthesis of Vitamin A Aldehyde. In: Nature. 1947, 160, S. 189, doi:10.1038/160189a0.
- ↑ James G Morris: "Idiosyncratic nutrient requirements of cats appear to be diet-induced evolutionary adaptations".Nutrition Research Reviews (2002), 15:153-168 Cambridge University Press [1]

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-A11
- ATC-D10
- ATC-R01
- ATC-S01
- Gesundheitsschädlicher Stoff
- Stoff mit Verdacht auf reproduktionstoxische Wirkung
- Allylalkohol
- Vitamin
- Polyen
- Cyclohexen
- Retinoid
- Arzneistoff
Wikimedia Foundation.