- tert-Leucin
-
Strukturformel 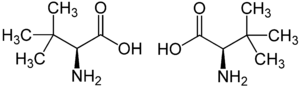
L-tert-Leucin (links) bzw. D-tert-Leucin (rechts) Allgemeines Name tert-Leucin Andere Namen - (S)-(+)-2-Amino-3,3-dimethylbutansäure
- L-(+)-α-Amino-3,3-dimethylbutansäure
- (S)-(+)-tert-Leucin
- (R)-(−)-tert-Leucin
- D-(−)-α-Amino-3,3-dimethylbutansäure
- Terleucin
- 2-Adba
- 3-Methylvalin
- tert-Butylglycin
Summenformel C6H13NO2 CAS-Nummer - 20859-02-3 (L-Enantiomer)
- 26782-71-8 (D-Enantiomer)
PubChem 164608 Eigenschaften Molare Masse 131,18 g·mol−1 Aggregatzustand fest
Schmelzpunkt > 300 °C (Zersetzung) [1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze EU-Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22-24/25 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. tert-Leucin (Terleucin) ist eine chirale, nicht-proteinogene α-Aminosäure, von der die beiden Enantiomere L-tert-Leucin [Synonym: (S)-tert-Leucin] und D-tert-Leucin [Synonym: (R)-tert-Leucin] existieren. tert-Leucin gehört zusammen mit seinen Konstitutionsisomere Leucin, Isoleucin und Norleucin zur Stoffgruppe der Leucine. Strukturell kann tert-Leucin über die Substitution eines α-Wasserstoffatoms durch eine Aminogruppe (–NH2) von der 3,3-Dimethylbuttersäure abgeleitet werden.
Darstellung
L-tert-Leucin wird derzeit auf enzymatischem Wege im Tonnenmaßstab hergestellt und soll als chirales Zwischenprodukt unter anderem bei der Synthese von Medikamenten zur Behandlung von Krebs oder AIDS zum Einsatz kommen.[2]
Einzelnachweise
- ↑ a b c Datenblatt L-tert-Leucine bei Sigma-Aldrich, abgerufen am 29. Mai 2011.
- ↑ Informationen des Herstellers Degussa.
Wikimedia Foundation.
