- Norleucin
-
Strukturformel 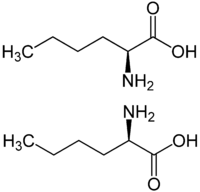
L-Norleucin (oben) und D-Norleucin (unten) Allgemeines Name L(+)-Norleucin Andere Namen - (S)-(+)-2-Aminohexansäure
- L(+)-α-Aminocapronsäure
- (S)-(+)-Norleucin
- (S)-Norleucin
- L-Norleucin
Summenformel C6H13NO2 CAS-Nummer 327-57-1 PubChem 21236 DrugBank DB04419 Kurzbeschreibung farblose Blättchen[1]
Eigenschaften Molare Masse 131,18 g·mol−1 Aggregatzustand fest
Schmelzpunkt 301 °C (Zersetzung)[1]
Löslichkeit schlecht in Wasser (16 g·l−1 bei 23 °C)[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [3] 
Achtung
H- und P-Sätze H: 317 EUH: keine EUH-Sätze P: 280 [3] EU-Gefahrstoffkennzeichnung [3] 
Reizend (Xi) R- und S-Sätze R: 43 S: 36/37 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Norleucin ist eine nicht-proteinogene chirale α-Aminosäure und wurde von Adolf Weil entdeckt. Es gibt zwei Enantiomere: L-Norleucin [Synonym: (S)-Norleucin] und D-Norleucin [Synonym: (R)-Norleucin]. Strukturell leitet sich Norleucin durch Substitution eines α-Wasserstoffatoms durch eine Aminogruppe (–NH2) von der Capronsäure ab. Leucin, Isoleucin und tert-Leucin sind Konstitutionsisomere.
Darstellung
Das Racemat erhält man durch Umsetzung von 2-Bromhexansäure mit NH3 in wässriger Lösung (50 °C, 30 h).[4]
Verwendung
Norleucin wird zur experimentellen Untersuchung von Proteinstrukturen und -funktionen verwendet. Aminoacyl-tRNA-Synthetasen können getäuscht werden, indem man ihnen anstelle ihrer normalen Substrate bestimmte unbiologische Aminosäuren anbietet. So werden Ethionin und Norleucin in solche Positionen in Proteine eingebaut, die normalerweise Methionin einnehmen würde.[5]
Einzelnachweise
- ↑ a b Hermann Römpp, Jürgen Falbe und Manfred Regitz: Römpp Lexikon Chemie, 9. Auflage, Georg Thieme Verlag, Stuttgart 1992.
- ↑ Datenblatt Norleucin bei Acros, abgerufen am 19. Februar 2010.
- ↑ a b c Datenblatt L-Norleucine bei Sigma-Aldrich, abgerufen am 16. April 2011.
- ↑ K. Peter C. Vollhardt, Neil E. Schore: Organische Chemie, 4. Auflage, Wiley-VCH, Weinheim 2005, ISBN 978-3-527-31380-8, S. 997.
- ↑ Albert L. Lehninger: Biochemie, 2. Auflage, VCH, Weinheim 1983, ISBN 3-527-25688-1, S. 767–768.
Kategorien:- Sensibilisierender Stoff
- Reizender Stoff
- Aminosäure
Wikimedia Foundation.
