- Cuminaldehyd
-
Strukturformel 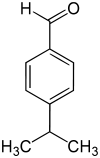
Allgemeines Name Cuminaldehyd Andere Namen - 4-Isopropylbenzaldehyd
- p-Isopropylbenzaldehyd
- Cuminal
Summenformel C10H12O CAS-Nummer 122-03-2 PubChem 326 Eigenschaften Molare Masse 148,20 g·mol−1 Aggregatzustand flüssig
Dichte 0,977 g·cm−3 (25 °C)[1]
Siedepunkt Brechungsindex 1,529 (20 °C)[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 
Achtung
H- und P-Sätze H: 302-315-319-335 EUH: keine EUH-Sätze P: 261-305+351+338 [1] EU-Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22-36/37/38 S: 26-36 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Cuminaldehyd (4-Isopropylbenzaldehyd) leitet sich strukturell von Benzaldehyd bzw. Cumol (Isopropylbenzol) ab und gehört zur großen Stoffgruppe der Terpene. Es ist ein Bestandteil ätherischer Öle wie Eukalyptus, Myrrhe, Kassia, Kümmel und andere. Es besitzt einen angenehmen Geruch und wird kommerziell in Parfums und anderen Kosmetika verwendet.
Inhaltsverzeichnis
Darstellung
Cuminaldehyd kann synthetisch durch die Reduktion von 4-Isopropylbenzoylchlorid oder durch Formylierung von Cumol hergestellt werden.
Eigenschaften
Cuminaldehyd ist der biologisch aktive Bestandteil des Kernöls von Kreuzkümmel (Cuminum cyminum). Die aus diesen Samen gewonnenen Substanzen besitzen eine hemmende Wirkung in vitro bei Ratten gegen Aldosereduktase und Alpha-Glucosidase. Diese hemmende Wirkung deutet auf eine potentielle Anwendung als Antidiabetikum hin.[2] Das Terpenoid Cuminaldehyd erfährt bei der Biotransformation in Säugetieren meist Reduktion aber nicht Oxidation.[3] Es gehört zu den flüchtigen Verbindungen des Kümmelaromas und lässt sich in Spuren in Blut und Milch von Schafen nachweisen, deren Futter u. a. Kümmelsamen zugesetzt wurden.[4]
Siehe auch
Einzelnachweise
- ↑ a b c d e f Datenblatt Cuminaldehyd bei Sigma-Aldrich, abgerufen am 22. April 2011.
- ↑ H. S. Lee: „Cuminaldehyde: Aldose Reductase and alpha-Glucosidase Inhibitor Derived from Cuminum cyminum L. Seeds“, in: J. Agric. Food Chem., 2005 Apr 6, 53 (7), S. 2446–5240; PMID 15796577.
- ↑ T. Ishida, M. Toyota, Y. Asakawa: „Terpenoid biotransformation in mammals. V. Metabolism of (+)-citronellal, (±)-7-hydroxycitronellal, citral, (−)-perillaldehyde, (−)-myrtenal, cuminaldehyde, thujone, and (±)-carvone in rabbits“, in: Xenobiotica, 1989 Aug, 19 (8), S. 843–855; PMID 2815827.
- ↑ M. Désage, B. Schaal, J. Soubeyrand, P. Orgeur, J. L. Brazier: „Gas chromatographic-mass spectrometric method to characterise the transfer of dietary odorous compounds into plasma and milk“, in: J. Chromatogr. B, Biomed Appl., 1996 Apr 12, 678 (2), S. 205–210; PMID 8738023.
Literatur
- Alfred Raab: „Mittheilungen: Ueber einige Derivate des Cuminaldehyds“, in: Berichte der deutschen chemischen Gesellschaft, 1875, 8 (2), S. 1148–1152; doi:10.1002/cber.18750080273.
Weblinks
- Human Metabolome Database: Cuminaldehyde (HMDB02214)
Wikimedia Foundation.
