- Capsid
-
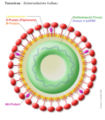
Als Kapsid oder Capsid (von lat. capsula: kleine Kapsel) bezeichnet man eine komplexe, regelmäßige Proteinstruktur bei Viren, die der Verpackung des Virusgenoms dient. Ein Kapsid ist aus einer festgelegten Anzahl von Protein-Untereinheiten, den Kapsomeren, aufgebaut. Bei unbehüllten Viren bildet das Kapsid die äußerste Struktur des Virus und ist damit für die Anheftung und das Eindringen in die Wirtszelle verantwortlich; bei behüllten Viren interagiert das Kapsid mit der äußeren Virushülle und verleiht ihr häufig erst die nötige Stabilität.
Die Anordnung der Proteine eines Kapsids basiert auf verschiedenen Symmetrien und ist sehr vielgestaltig. Diese unterschiedlichen Strukturen und Symmetrien von Kapsiden haben wiederum Auswirkungen auf die biologischen Eigenschaften wie die Pathogenität, die Art der Virusvermehrung (Replikation) und die Umweltstabilität. Die Struktur des Kapsids dient auch als Kriterium der Einteilung von Viren innerhalb der Virus-Taxonomie.Inhaltsverzeichnis
Entdeckung
Schon in den 1950er Jahren wurde von Francis Crick und James Watson angenommen, dass die Verpackung der Nukleinsäure von Viren aus vielen identischen Untereinheiten bestehen müsse und diese notwendigerweise symmetrisch angeordnet seien.[1] Dies ergibt sich aus der Überlegung, dass die Information auf einer Nukleinsäure niemals dazu ausreichen könnte, von einem einzigen großen Protein verpackt zu werden, das gleichzeitig durch die Nukleinsäure selbst codiert wird. Die genetische Information wird durch viele identische Proteine also mehrfach genutzt.
Kapsomer
Als Kapsomer (pl. Kapsomere) bezeichnet man die kleinste regelmäßige Einheit, aus der ein Kapsid aufgebaut ist und die dessen Symmetrie bestimmt. Im einfachsten Fall besteht ein Kapsid aus identischen Kapsomeren, die wiederum nur aus einem Proteinmolekül bestehen. Sehr häufig jedoch besteht ein Kapsomer aus zwei bis fünf verschiedenen Proteinen, die sich zu einem regelmäßigen Kapsid zusammenlagern. Es kann auch aus verschiedenen Kapsomeren aufgebaut sein, z. B. bestehen Adenoviren aus zwei unterschiedlichen Kapsomeren (Pentone und Hexone), die wiederum selbst aus verschiedenen Virusproteinen bestehen.
Die einzelnen Untereinheiten, aus denen ein Kapsomer wiederum aufgebaut sein kann, werden gelegentlich auch als Protomere bezeichnet.
Bei einer vorgegebenen Genomsequenz eines Virus können jene Proteine, die das Kapsomer bilden, sehr leicht erkannt werden, da diese in bestimmten Abschnitten eine hohe Konzentration von positiv geladenen bzw. basischen Aminosäuren (Arginin, Lysin, Histidin) beinhalten. Diese basischen Proteindomänen der Kapsidproteine (Coreproteine) sind zur nicht-kovalenten Bindung an die negativ geladene virale Nukleinsäure notwendig, die verpackt werden soll.
Symmetrieformen
Ikosaedrische Symmetrie
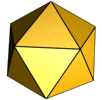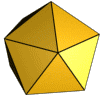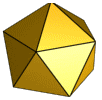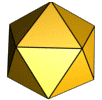
Die häufigste Symmetrie eines Kapsids ist ein regelmäßiger Ikosaeder (Zwanzigflächner), da dieser unter allen regelmäßigen Vielflächnern (Polyeder) bei gegebener Kantenlänge das größte Volumen beinhaltet. Die Kantenlänge wird durch die Größe der Kapsomere und ihre Anzahl bestimmt. Bei der Darstellung von Virionen im Elektronenmikroskop (EM) oder mittels Röntgenstrukturanalyse entspricht jedoch bei vielen Viruskapsiden das Erscheinungsbild, also die äußere Gestalt, nicht einem Ikosaeder, sondern ist meist kugelförmig, teilweise mit herausragenden Proteinschleifen (spikes) versehen. Verbindet man aber gleiche Molekülpositionen der Kapsomere miteinander, so findet man eine ikosaedrische Anordnung der Kapsomere. Daher gilt es zwischen dem Begriff der Symmetrie eines Kapsids und der Form (Morphologie) eines Kapsids gut zu unterscheiden. Bei einigen Viren kann die innere Symmetrie eines Ikosaeders auch sofort an der äußeren Form erkannt werden, z. B. bei Mitgliedern der Familie Adenoviridae oder einigen Bakteriophagen.
Die meisten viralen Kapside mit ikosaedrischer Symmetrie sind isometrisch, d. h. alle Seitenkanten des Ikosaeders sind gleich lang. Hiervon gibt es wenige abweichende Beispiele (z. B. der T4-Phage und seine Familie Myoviridae), wobei der Ikosaeder langgestreckt erscheint und damit im geometrischen Sinne kein Ikosaeder mehr ist sondern ein fünfeckiges, bipyramidales Antiprisma. Virologen sprechen bei dieser Form jedoch trotzdem von einem nicht-isometrischen Ikosaeder.Symmetrieachsen
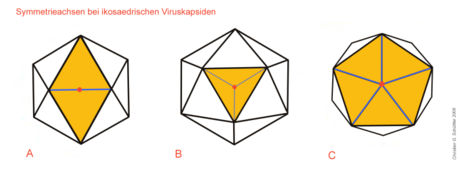
Für die Struktur des Ikosaeders sind drei Symmetrieachsen charakteristisch (rote Punkte in der obigen Abbildung), die eine Rotationssymmetrie zeigen: durch die Seitenkanten verläuft eine Symmetrieachse mit zweistrahliger (180°) Symmetrie (Bild A), durch die dreieckigen Seitenflächen eine dreistrahlige (120°, Bild B) und durch die Ecken eine fünfstrahlige (72°, Bild C). Die entsprechende Symmetrie weisen die Kapsomere oder ihre Anordnung auf dem Ikosaeder auf. So kann ein Kapsid aus Kapsomeren aufgebaut sein, die eine dreistrahlige oder eine fünfstrahlige Symmetrie aufweisen, häufig zeigen die Kapsomerformen innerhalb eines Kapsids je nach Position auch verschiedene Symmetrien, da sie meist aus zwei, drei oder fünf identischen Proteinuntereinheiten bestehen. Die Anordnung der Kapsomere zu einer bestimmten Rotationssymmetrie ist nicht immer zwangsläufig durch die Struktur der Proteine vorgegeben. So gibt es bei manchen Viruskapsiden auch verschiedene Möglichkeiten der Anordnung zu einem Ikosaeder, was sich auch in der Bildung unterschiedlicher Viruspartikel mit gering verschiedenen Durchmessern bei ein und demselben Virus zeigt. So bestehen die Kapside von natürlichen Virionen des Hepatitis-B-Virus überwiegend aus 180 Kapsomeren (T=3, siehe unten), etwa 20 % der Kapside jedoch aus 240 Kapsomeren (T=4).[2] Die biologische Bedeutung unterschiedlicher Kapsidsymmetrien bei ein und demselben Virus ist bislang nicht geklärt.Triangulationszahl
 Felix als Kapsid mit der Triangulationszahl T=1
Felix als Kapsid mit der Triangulationszahl T=1Zur genaueren Beschreibung eines ikosaedrischen Kapsids, wurde 1962 von Donald Caspar und Aaron Klug eine geometrische Kennzahl eingeführt,[3] die sogenannte Triangulationszahl (T). Mit ihr kann man die Größe und die Komplexität eines Kapsids beschreiben.
Durch Zusammenlagerung von drei identischen Molekülen eines beliebigen unregelmäßigen, nicht-symmetrischen Proteins kann ein gleichseitiges (rotationssymmetrisches) Dreieck gebildet werden. Diese Anordnung ist die kleinstmögliche symmetrische Einheit zur Ausbildung eines ikosaedrischen Kapsids. Da ein solches regelmäßiges Dreieck also aus mindestens drei Untereinheiten aufgebaut ist und ein Ikosaeder aus zwanzig solcher regelmäßiger Dreiecke besteht, sind mindestens 3x20=60 solcher Untereinheiten zur Ausbildung der einfachsten ikosaedrischen Symmetrie notwendig. Diese Mindestzahl von 60 wird durch die Triangulationszahl T=1 beschrieben. Größere und komplexere Kapside besitzen nur ganzzahlige Vielfache von 60, also z. B. häufig 180 (T=3), 240 (T=4), 960 (T=16). Die geometrisch möglichen Triangulationszahlen ergeben sich aus der Formel T=h² + hk + k², wobei h und k ganze Zahlen sind.Helikale Symmetrie
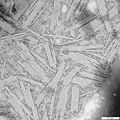
Bei einigen Viren lagern sich die Kapsomere schraubenförmig zu einer helikalen Quartärstruktur um die zu verpackende Nukleinsäure; dabei bilden sie nach außen eine längliche Zylinderform. Der Durchmesser eines helikalen Kapsids ist durch die Größe der Kapsomere festgelegt, die Länge des Zylinders ist direkt abhängig von der Länge der zu verpackenden Nukleinsäure.
Mehrere ringförmige, helikale Kapside (blau) bei Arenaviren
Unbehüllte (nackte) helikale Kapside kommen nur bei einigen Pflanzenviren (z. B. Tabakmosaikvirus, Lily-Mottle-Virus) und Bakteriophagen (Familie Inoviridae) vor, während Viren mit behülltem helikalem Kapsid bei Tieren weit verbreitet sind. Wichtige Krankheitserreger mit helikalem Kapsid sind beispielsweise die Influenzaviren, die Paramyxoviridae (z. B. das Mumpsvirus und Masernvirus), die Bunyaviridae oder Rhabdoviridae (z. B. das Tollwutvirus). Eine Sonderform der helikalen Symmetrie liegt bei der Virusgattung Torovirus vor. Hier bildet sich aus einem länglichen helikalen Kapsid ein geschlossener Ring, der die geometrische Form eines Torus zeigt.
Komplexe oder keine Symmetrie
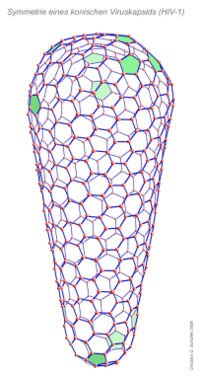 Komplexes, konisches Kapsid bei HIV-1
Komplexes, konisches Kapsid bei HIV-1Manche Kapside besitzen weder eine eindeutig ikosaedrische noch helikale Symmetrie, trotzdem zeigt ihre Form eine regelmäßige Struktur. Dies ist besonders bei Mitgliedern der Familie Poxviridae (Pockenviren) zu beobachten. Daher wird die Symmetrie dieser Viren als „komplex“ bezeichnet.
Eine Sonderstellung innerhalb der komplexen Symmetrien nehmen die konischen (kegelförmigen) Nukleokapside bei Retroviren, z. B. dem HIV-1, ein. Das Coreprotein dieses Virus kann in vitro Röhren mit helikaler Symmetrie ausbilden, jedoch auch die natürliche Form der konischen, geschlossenen Röhre annehmen. Dabei zeigt sich, dass dieses Kapsid aus einem Netzwerk von Sechsecken aufgebaut ist, das durch 12 Netzmaschen mit fünfeckiger Anordnung unterbrochen ist (in der Abbildung grün markiert).[4] Von den zwölf fünfeckigen Lücken befinden sich sieben am breiten und fünf am schmalen Ende des Konus. Damit folgt diese Netzwerk-Symmetrie einem mathematischen Theorem von Leonhard Euler, demzufolge eine geschlossene Oberfläche, die durch Sechsecke bedeckt werden soll, stets mindestens zwölf fünfeckige Lücken aufweist. Durch diese sehr variablen Winkelverhältnisse der Kapsomere zueinander und die durch die Fünfecke entstehenden Stellen mit geringerer Stabilität wird wahrscheinlich die Freisetzung des Retrovirus-Genoms in den Zellkern erst ermöglicht.
Darüber hinaus gibt es Viren, bei denen keine eindeutige Kapsidform nachgewiesen werden konnte. Diese Viren verfügen jedoch über Proteine mit den oben beschriebenen basischen Proteindomänen, die zwischen Nukleinsäure und Virushülle vermitteln und meist von innen in der Virushülle verankert sind. Mit dieser Verankerung in der Hülle sind sie mit den sogenannten Matrixproteinen verwandt, die bei anderen Viren (z. B. den Herpesviridae und Paramyxoviridae) zusätzlich zu einem Kapsid die Hülle von innen auskleiden; strenggenommen dürfte man nicht von einem Kapsid sprechen. Diese Proteine werden aus historischen Gründen meist als Coreproteine bezeichnet. Bekannteste Beispiele hierfür sind das Hepatitis-C-Virus und das Bovine Virusdiarrhoe-Virus BVDV.
Kapsid und Nukleokapsid
Häufig werden die Begriffe Kapsid und Nukleokapsid fälschlicherweise synonym verwendet. Nur ein Kapsid, das direkt mit der Nukleinsäure assoziiert ist, ist auch ein Nukleokapsid. Es gibt Viren (z. B. das Humane Immundefizienz-Virus), bei denen sich innerhalb eines äußeren Kapsids ein zweites befindet; hier wird nur dieses innerste als Nukleokapsid (oder Core) bezeichnet. Im Inneren eines Kapsids kann sich die Nukleinsäure zusätzlich mit basischen Proteinen (z. B. zellulären Histonen) assoziieren oder mit Proteinen kovalent verknüpft sein. In diesem Falle spricht man von einem Nukleoprotein-Komplex.
Energetische Betrachtung der Kapsidbildung
Kapside können sich innerhalb einer Zelle oder experimentell als gereinigte Proteinlösung der Kapsomere spontan und ohne Energieverbrauch bilden; dies wird auch oft als Selbstassemblierung (engl. self-assembly ) bezeichnet. Zum ersten Mal konnte die spontane Kapsidbildung beim Tabakmosaikvirus beobachtet werden; in vitro gelang dies auch später bei animalen Viren wie z. B. den Alphaviren.[5]
Bei einer großen Anzahl von Viren gelang diese Kapsidbildung in vitro jedoch nicht. Man fand, dass zur Zusammenlagerung der Kapsomere und zu deren korrekter Faltung zum Teil zelluläre Proteine notwendig sind (sogenannte Chaperone)[6] oder erst eine Assoziation mit Nukleinsäure zur Kapsidbildung führt.
Ausgehend von der Tatsache, dass eine Kapsidbildung spontan erfolgen kann und die Symmetrie des Ikosaeders besonders oft vorkommt, nahm man bisher an, dass die Kapsidstruktur der energetisch günstigste Zustand für die Kapsomere darstellt. Tatsächlich zeigen neuere Untersuchung, dass Kapside eher einem metastabilen energetischen Zustand entsprechen. [7] Dies würde auch zum Teil erklären, warum Kapside sich bei der Ausschleusung des Virus aus der Zelle zunächst zusammenlagern, hingegen bei Eintritt in die Zelle die gleichen Kapside wieder spontan zerfallen, um die virale Nukleinsäure freizusetzen. Der energetisch instabilste und limitierende Schritt für das self-assembly eines ikosaedrischen Kapsids scheint der Einbau der letzten Kapsomere zur Komplettierung zu sein. [8] Dieser metastabile Zustand wird auch dadurch begünstigt, dass ein Kapsid seine Stabilität lediglich aus sehr schwachen Wechselwirkungen der Kapsomere gewinnt.[9]
Manche Kapside werden nach dem Zusammenbau auf der Außenseite oder auch der Innenseite (z. B. beim Kapsid des Hepatitis-B-Virus) durch mitverpacktes ATP und Phosphokinasen phosphoryliert, zum Teil auch durch zelluläre Enzyme glykosyliert; diese Modifikationen scheinen auch die Stabilität bzw. gewünschte Instabilität der Kapside zu beeinflussen.
Ein besonderes Merkmal mancher unbehüllter Viren oder der in vitro synthetisierten Kapside behüllter Viren ist die Möglichkeit zu kristallisieren. Diese Beobachtung führte schon in den 1940er Jahren zu Diskussionen über die Zuordnung von Viren als Lebensform, da sonst nur unbelebte Stoffe die Eigenschaft der Kristallbildung zeigen. Kristallisierte Kapside sind bei der Erforschung der Virusstruktur durch die Röntgenstrukturanalyse unerlässlich.
Biologische Bedeutung von Kapsiden
Neben dem Schutz des viralen Genoms vor überall präsenten DNA- und RNA-spaltenden Enzymen (Nukleasen) und der Formgebung bei behüllten Viren, haben Kapside einige besondere biologische Funktionen und Eigenschaften:
- Bei unbehüllten Viren bildet das Kapsid die Oberfläche eines Virions. Dadurch ist es direkt der Abwehr durch das Immunsystem ausgesetzt und wirkt als Antigen. Um dem Immunsystem zu entgehen, verändern Viren häufig ihre Oberflächenepitope, was jedoch bei nackten Kapsiden nur sehr eingeschränkt möglich ist, da etliche Veränderungen der Kapsidproteine auch zum Verlust der Stabilität oder einer Beeinträchtigung des self-assembly führen. Unbehüllte Viren sind daher in der Regel weniger variabel in den Oberflächenepitopen als behüllte.
- Da regelmäßig angeordnete Proteine ein wesentlich stärkeres Antigen darstellen als unregelmäßig angeordnete, eignen sich intakte Kapside besonders gut als Material für Impfungen.
- Das Kapsid unbehüllter Viren vermittelt ebenfalls die Bindung an Rezeptoren der Zielzelle, um den Eintritt in die Zelle einzuleiten. Bei einigen behüllten DNA-Viren sorgt ein spezieller Transport des Kapsids an die Kernporen für das Eindringen des Virusgenoms in den Zellkern.
- Durch die Fähigkeit von Kapsiden, als Transportvehikel für Nukleinsäure in Zellen zu dienen, sind in vitro erzeugte Kapside, sogenannte Virus-like particles (VLPs), von besonderem Interesse in der Gentechnik und Gentherapie.
Quellen
Literatur
- D. M. Knipe, P. M. Howley (Hrsg.): Fields’ Virology. 5. Auflage, 2 Bände, Philadelphia 2007 ISBN 0-7817-6060-7
- S. J. Flint, L. W. Enquist, V. R. Racaniello und A. M. Skalka: Principles of Virology. Molecular Biology, Pathogenesis, and Control of Animal Viruses. 2. Auflage, ASM-Press Washington D.C. 2004, ISBN 1-55581-259-7
- A. J. Cann: Principles of Molecular Virology. 3. Auflage, Academic Press 2001 ISBN 0-12-158533-6
- A. Granoff, R. G. Webster (Hrsg.): Encyclopedia of Virology. San Diego 1999 (Band 1-3) ISBN 0-12-227030-4
- R. H. Cheng und T. Miyamura (Hrsg.): Structure-based study of viral replication. Singapore 2008 ISBN 981-270-405-1
- Roya Zandi, David Reguera et al.: Origin of icosahedral symmetry in viruses. PNAS (2004) 101,44: 15556-60
Einzelnachweise
- ↑ Francis Crick und James Watson: Structure of Small Viruses. Nature (1956) 177: S. 473-475 PMID 13309339
- ↑ M. Newman, F. M. Suk, M. Cajimat, P. K. Chua, C. Shih: Stability and morphology comparisons of self-assembled virus-like particles from wild-type and mutant human hepatitis B virus capsid proteins. Journal of Virology (2003) 77(24): S. 12950-12960 PMID 14645551
- ↑ Donald L. D. Caspar, Aaron Klug: Physical Principles in the Construction of Regular Viruses. Cold Spring Harbor Symposia on Quantitative Biology XXVII, Cold Spring Harbor Laboratory, New York (1962) S. 1-24
- ↑ B. K. Ganser, S. Li, V. Y. Klishko et al.: Assembly and analysis of conical models for the HIV-1 core. Science (1999) 283, 5398: 80-83. PMID 9872746
- ↑ Hiebert E, Bancroft JB, Bracker CE: The assembly in vitro of some small spherical viruses, hybrid viruses, and other nucleoproteins. Virology (1968) 3: S. 492-508 PMID 5651027
- ↑ Lingappa JR, Martin RL, Wong ML, Ganem D, Welch WJ, Lingappa VR: A eukaryotic cytosolic chaperonin is associated with a high molecular weight intermediate in the assembly of hepatitis B virus capsid, a multimeric particle. Journal of Cell Biology (1994) 125(1): S. 99-111 PMID 7908022 Link
- ↑ Robijn F. Bruinsma, William M. Gelbart: Viral Self-Assembly as a Thermodynamic Process. Physical Review Letters (2003) 90, 24: 248101 (e-pub) PMID 12857229
- ↑ Nguyen HD, Reddy VS, Iii CL: Deciphering the kinetic mechanism of spontaneous self-assembly of icosahedral capsids. Nano Lett. (2007) Feb;7(2):338-344 PMID 17297998
- ↑ Ceres P, Zlotnick A: Weak protein-protein interactions are sufficient to drive assembly of hepatitis B virus capsids. Biochemistry (2002) Oct 1;41(39):11525-31 PMID 12269796
Weblinks
Wikimedia Foundation.