- Pyruvatkinase M2
-
Pyruvatkinase Isoform M2 —
Vorhandene Strukturdaten: 1t5a, 1zjh, 3bjf, 3bjt Masse/Länge Primärstruktur 530 Aminosäuren Sekundär- bis Quartärstruktur Homodimer, Homotetramer Kofaktor Magnesium, Kalium Isoformen L, R, M1, M2 Bezeichner Gen-Name PKM2 Externe IDs OMIM: 179050 UniProt: P14618 Enzymklassifikation EC, Kategorie 2.7.1.40 Kinase Reaktionsart Phosphorylierung Substrat ADP + Phosphoenolpyruvat Produkte ATP + Pyruvat Vorkommen Homologie-Familie Pyruvatkinase Übergeordnetes Taxon Euteleostomi Pyruvatkinase M2 (auch: Tumor M2-PK) ist ein Enzym im Menschen, das nur in fötalem und in Tumorgewebe vorkommt, und daher als Tumormarker dient.
Es ist eine Isoform der Pyruvatkinase mit der Bezeichnung M2 (abgekürzt M2-PK oder auch PKM2). Die Pyruvatkinase M2 ist ein Schlüsselenzym im Tumorstoffwechsel und kann in Stuhlproben zum Screening von kolorektalen Tumoren und im EDTA-Plasma zur Therapie und Verlaufskontrolle verschiedener Tumorerkrankungen eingesetzt werden.
Die Tumor-M2-Pyruvatkinase ist kein organspezifischer Tumormarker, wie beispielsweise PSA, vielmehr reflektiert der Gehalt an Tumor M2-PK im Stuhl und im EDTA-Plasma als Biomarker den spezifischen Stoffwechselzustand der Tumoren.
Inhaltsverzeichnis
Labortest
Zur Quantifizierung der Tumor M2-PK im Stuhl und im EDTA-Plasma steht ein Sandwich-ELISA zur Verfügung, der auf zwei monoklonalen Antikörpern beruht, die spezifisch die Tumor M2-PK (dimere Form der M2-PK) erkennen.
Tumor-M2-PK-Screening zur Früherkennung von kolorektalen Tumoren und Polypen
Klinische Studien aus Deutschland, England und Irland, in denen der Nachweis der Tumor M2-PK im Stuhl als Stoffwechsel-Biomarker zur Früherkennung von kolorektalen Tumoren getestet wurde, ergaben für die Tumor M2-PK Sensitivitäten zwischen 78 und 97 %. Dies bedeutet, dass von 100 an kolorektalen Tumoren erkrankten Personen in den verschiedenen Studien zwischen 78 und 97 durch den Tumor M2-PK Test erkannt wurden. Für Polypen > 1 cm lag die Sensitivität bei 60 %; für Polypen < 1 cm bei 25 %. Für alle Polypen ergab sich eine Sensitivität von 40 %.
Aufgrund der generell höheren Teilnahmebereitschaft an Vorsorgeuntersuchungen mit nicht invasiven Verfahren stellt der Nachweis der Tumor M2-PK im Stuhl in Kombination mit der koloskopischen Abklärung positiver Befunde eine Möglichkeit zur Verbesserung der Früherkennung kolorektaler Karzinome dar.
Tumor-M2-PK-Messungen zur Therapie- und Verlaufskontrolle bei verschiedenen Tumorerkrankungen
Studien internationaler Arbeitsgruppen haben gezeigt, dass der Gehalt an Tumor M2-PK im EDTA-Plasma von Patienten mit Nierentumoren, Lungentumoren, Brusttumoren, Zervikaltumoren, Tumoren des Gastrointestinaltraktes (Oesophagus, Magen, Pankreas, Kolon und Rektum) sowie bei Melanomen signifikant ansteigt und mit dem Stadium der Tumore korreliert.
Die Kombination der Tumor M2-PK mit klassischen Tumormarkern, wie zum Beispiel, CEA, CA 19-9 und CA 72-4, kann die Sensitivität des Nachweises von Tumorerkrankungen deutlich erhöhen.
Ein wichtiges Anwendungsgebiet des Nachweises der Tumor M2-PK im EDTA-Plasma sind Verlaufskontrollen unter der Therapie, die es ermöglichen, den Erfolg oder Misserfolg einer Therapie frühzeitig zu erfassen und Prognosen über die Heilungschancen zu stellen.
Fallen die Tumor-M2-PK-Werte im EDTA-Plasma des Tumor-Patienten unter der Therapie ab und bleiben sie dauerhaft niedrig, deutet dies auf einen guten Erfolg der Therapie hin. Steigen die Tumor M2-PK-Werte während oder nach der Therapie an, ist dies ein deutlicher Hinweis darauf, dass sich ein Rezidiv und/oder Metastasen gebildet haben.
Erhöhte Tumor-M2-PK-Werte können auch bei schweren entzündlichen Erkrankungen auftreten und müssen differentialdiagnostisch ausgeschlossen werden.
Wissenschaftlicher Hintergrund zur Rolle der PKM2 im Tumor-Stoffwechsel
Die Pyruvatkinase katalysiert den letzten Schritt innerhalb der Glycolyse, die Dephosphorylierung von Phosphoenolpyruvat zu Pyruvat und ist für die Netto-Energiegewinnung in diesem Stoffwechselweg verantwortlich.
In Abhängigkeit von den unterschiedlichen metabolischen Aufgaben der verschiedenen Gewebe werden unterschiedliche Isoenzyme der Pyruvatkinase exprimiert.
Die M2-PK (PKM2) ist das charakteristische Pyruvatkinase-Isoenzym aller proliferierenden (sich teilenden) Zellen. Dazu gehören normal proliferierende Zellen, wie z. B. Fibroblasten, embryonale Zellen oder adulte Stammzellen und vor allem Tumorzellen.
Während der Tumorentstehung kommt es zu einem Wechsel im Isoenzymmuster der Zellen, wobei das jeweilige Gewebe-spezifische Isoenzym, wie zum Beispiel die L-PK in der Leber oder die M1-PK im Gehirn verschwindet und das Isoenzym Typ M2 vermehrt gebildet wird.
Bedeutung der tetrameren und dimeren Form der M2-PK im Tumor-Stoffwechsel
Die M2-PK kann in proliferierenden Zellen in zwei unterschiedlichen Zustandformen auftreten:
- in einer tetrameren Form, die aus vier Untereinheiten zusammengesetzt ist und
- in einer dimeren Form, die aus zwei Untereinheiten besteht.
Die tetramere Form der M2-PK hat eine hohe Affinität zum Substrat Phosphoenolpyruvat und ist unter physiologischen Bedingungen hochaktiv. Weiterhin ist die tetramere Form mit anderen Enzymen im Cytosol im sogenannten Glycolyse-Enzym-Komplex assoziiert, der durch die räumliche Nähe der Enzyme zueinander eine hocheffektive Umsetzung von Glucose zu Pyruvat und Lactat ermöglicht.
Liegt die M2-PK überwiegend in der hochaktiven tetrameren Form vor, wie dies in den meisten normal proliferierenden Zellen der Fall ist, wird die Glucose überwiegend unter Energieproduktion zu Pyruvat abgebaut.
Die dimere Form der M2-PK hat eine geringe Affinität zum Substrat und ist unter physiologischen Bedingungen nahezu inaktiv. Die dimere Form ist nicht im Glycolyse-Enzym-Komplex assoziiert.
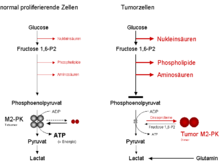
Liegt die M2-PK überwiegend in der wenig aktiven dimeren Form vor, wie dies in Tumorzellen der Fall ist, kommt es oberhalb der Pyruvatkinase Reaktion zu einem Rückstau aller Glycolyse-Zwischenprodukte. Diese stehen den Zellen als Ausgangsstoffe für aus der Glycolyse abzweigende Syntheseprozesse zur Verfügung. Zu diesen Synthesewegen gehören die Nukleinsäure-, Phospholipid- und Aminosäure-Synthese.
Nukleinsäuren, Phospholipide und Aminosäuren sind wichtige Zellbausteine, die hochteilungsaktive Zellen, wie dies Tumorzellen sind, dringend benötigen.
Aufgrund der Schlüsselstellung der Pyruvatkinase als letztes Enzym innerhalb der Glycolyse entscheidet somit das Tetramer : Dimer Verhältnis der M2-PK, ob die Glucose-Kohlenstoffatome unter Energiegewinnung zu Pyruvat und Lactat abgebaut werden (tetramere Form) oder in Synthesewege eingeschleust werden.
Da in Tumorzellen generell die dimere Form der M2-PK überwiegt, wurde die dimere Form der M2-PK als Tumor M2-PK bezeichnet.
Die Dimerisierung der M2-PK wird in Tumorzellen durch direkte Interaktion der M2-PK mit verschiedenen Oncoproteinen induziert.
Allerdings ist das Verhältnis von Tetramer zu Dimer der M2-PK in Tumorzellen kein statischer Zustand. Sauerstoffmangel oder hochangestaute Stoffwechsel-Zwischenprodukte, wie zum Beispiel das Glycolyse-Zwischenprodukt Fructose 1,6-P2 oder die Aminosäure Serin, induzieren die Reassozation der dimeren Form der M2-PK zur tetrameren Form. In der Folge wird durch die Reaktivierung der M2-PK die Glucose solange unter Energieproduktion zu Pyruvat und Lactat abgebaut, bis die Fructose 1,6-P2-Spiegel unter einen bestimmten Grenzwert fallen und die M2-PK wieder in die dimere Form dissoziiert. Der Oscillationscyclus startet erneut, wenn die Fructose 1,6-P2-Spiegel wieder über ihren Signal-Spiegel steigen und die Tetramerisierung der M2-PK induzieren.
Liegt die M2-PK überwiegend in der wenig aktiven dimeren Form vor, kann die Energie über den Abbau der Aminosäure Glutamin zu Aspartat, Pyruvat und Lactat (= Glutaminolyse) bereitgestellt werden.
Die in Tumorzellen beobachtete erhöhte Bildung von Lactat in Gegenwart von Sauerstoff wird als Warburg-Effekt bezeichnet.
Quellen
Tumor M2-PK im Stuhl
- U Haug, S Hundt and H Brenner(2008):"Sensitivity and specificity of faecal tumour M2 pyruvate kinase for
detection of colorectal adenomas in a large screening study" British Journal of Cancer (2008) 99, 133 – 135.doi:10.1038/sj.bjc.6604427
- Hardt PD, Mazurek S, Toepler M, Schlierbach P, Bretzel RG, Eigenbrodt E, Kloer HU (2004): Faecal tumour M2 pyruvate kinase: a new, sensitive screening tool for colorectal cancer. Brit. J. Cancer 91: 980-984. PMID 15266315
- Koss K, Maxton D, Jankowski JAZ. The potential use of fecal dimeric M2 pyruvate kinase (Tumor M2-PK) in screening for colorectal cancer (CRC). Abstract from Digestive Disease Week, May 2005; Chicago, USA.
- Mc Loughlin R, Shiel E, Sebastian S, Ryan B, O´Connor HJ, O´Morain C. Tumor M2-PK, a novel screening tool for colorectal cancer. Abstract from Digestive Disease Week, May 2005, Chicago/USA
- Tonus C, Neupert G, Sellinger M (2006): Colorectal cancer screening by non-invasive metabolic biomarker fecal M2-PK. World J Gastroenterol 12: 7007-7011. PMID 17109496
- Tonus C, Neupert G, Witzel K (2009): The faecal tumour M2-PK screening test for invasive & pre-invasive colorectal cancer: estimated specificity & results as a function of age for a study population of 4854 volunteers. Nowotwory J Oncol, 59: 32e-37e.
Tumor M2-PK im Plasma
- Cerwenka H, Aigner R, Bacher H, Werkgartner G, El-Shabrawi A, Quehenberger F, Mischinger HJ (1999) TUM2-PK (pyruvate kinase type tumor M2), CA19-9 and CEA in patients with benign, malignant and metastasizing pancreatic lesions. Anticancer Res. 19: 849-52. PMID 10216504
- Kaura B, Bagga R, Patel FD (2004): Evaluation of the pyruvate kinase isoenzyme tumor (Tu M2-PK) as a tumor marker for cervical carcinoma. J. Obstet. Gynaecol. Res. 30: 193-196. PMID 15210041
- Kim CW, Kim JI, Park SH, Han JY, Kim JK, Chung KW, Sun, HS (2003): Usefulness of plasma tumor M2-pyruvate kinase in the diagnosis of gastrointestinal cancer. Korean J. Gastroenterol. 42: 387-393. PMID 14646575
- Lüftner D, Mesterharm J, Akrivakis C, Geppert R, Petrides PE, Wernecke KD, Possinger K (2000): Tumor M2-pyruvate kinase expression in advanced breast cancer. Anticancer Res. 20: 5077-5082. PMID 11326672
- Oremek GM, Teigelkamp S, Kramer W, Eigenbrodt E, Usadel KH (1999): The pyruvate kinase isoenzyme tumor M2 (Tu M2-PK) as a tumor marker for renal carcinoma. Anticancer Res. 19: 2599-2601. PMID 10470201
- Schneider J, Morr H, Velcovsky HG, Weisse G, Eigenbrodt E (2000): Quantitative detection of tumor M2-pyruvate kinase in plasma of patients with lung cancer in comparison to other lung diseases. Cancer Detec. Prev. (2000), 24: 531-535. PMID 11198266
- Schneider J, Schulze G (2003): Comparison of Tumor M2-pyruvate kinase (Tumor M2-PK), carcinoembryonic antigen (CEA), carbohydrate antigens CA 19-9 and CA 724 in the diagnosis of gastrointestinal cancer. Anticancer Res. 23: 5089-5095. PMID 14981971
- Ugurel S, Bell N, Sucker A, Zimpfer A, Rittgen W, Schadendorf D (2005): Tumor type M2 pyruvate kinase (TuM2-PK) as a novel plasma tumor marker in melanoma. Int. J. Cancer 117: 825-830. PMID 15957165
- Ventrucci M, Cipolla A, Racchini C, Casadei R, Simoni P, Gullo L (2004): Tumor M2-pyruvate kinase, a new metabolic marker for pancreatic cancer. Dig. Dis. Sci. 49: 1149-1155. PMID 15387337
- Wechsel HW, Petri E, Bichler KH, Feil G (1999): Marker for renal carcinoma (RCC): The dimeric form of pyruvate kinase type M2 (Tu M2-PK). Anticancer Res. 19: 2583-2590. PMID 10470199
- Zhang B, Chen JY, Chen D-D, Wang G-B, Shen P (2004): Tumor type M2 pyruvate kinase epxression in gastric cancer, colorectal cancer and controls. World J. Gastroenterol. 10: 1643-1646. PMID 15162541
Wissenschaftlicher Hintergrund zur Tumor M2-PK
- Mazurek S, Boschek CB, Hugo F, Eigenbrodt E (2005): Pyruvate kinase type M2 and its role in tumor growth and spreading. Semin. Cancer Biol. 15: 300-308. PMID 15908230
Weblinks
- Die Tumor M2-PK als diagnostischer Biomarker (englisch)
- Das Pyruvatkinase-Isoenzym Typ M2 (englisch)
- Darmkrebs: Neuer Enzymtest zur Frühdiagnose
- Laborlexikon

Bitte den Hinweis zu Gesundheitsthemen beachten!
Wikimedia Foundation.