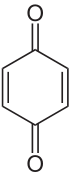
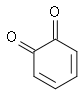
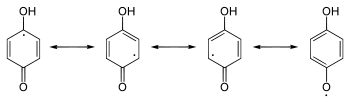
- Chinole
-
Chinone bilden eine große und wichtige Gruppe von organischen Verbindungen, die als Oxidationsprodukte von Aromaten, insbesondere von Phenolen, aufgefasst werden können. Der Name Chinon leitet sich von der Chinasäure ab, deren Oxidation u. a. zu Benzochinon führt. Im Allgemeinen sind Chinone Benzenderivate, bei denen unter Aufhebung der Aromatizität des Ringes an zwei Kohlenstoffatomen die Substituenten durch doppelbindigen Sauerstoff ersetzt wurden. Stoffe, deren chemische Struktur ein Chinon-Element enthält, nennt man chinoid, das Strukturelement selbst chinoides System. Die Reduktion von Chinonen liefert die zugehörigen Phenole, die auch Chinole genannt werden.
Die durchweg farbigen Chinone sind Oxidationsmittel, deren Redoxpotenzial durch Substituenten (Halogen-, Cyan-, Alkyl-, Hydroxy-Gruppen etc.) deutlich verändert wird. Man kann zwischen 1,2-(ortho-)Chinonen (z. B. PQQ) und 1,4-(para-)Chinonen (z. B. Anthrachinon) unterscheiden.
Durch den Ersatz des Sauerstoffs einer chinoiden Carbonyl-Gruppe durch =NH, =NOH, =N2 oder =CH2 leiten sich die Chinonimine, Chinonoxime, Chinondiazide und Chinonmethide ab.
Synonym steht Chinon in der Chemie für die Verbindung 1,4-Benzochinon, welche durch Oxidation aus 1,4-Dihydroxybenzol (Trivialname Hydrochinon) entsteht. Unter den Chinonen finden sich viele Gifte, aber auch ein breites Spektrum an lebensnotwendigen Vitalstoffen (z. B. Ubichinone, Phyllochinone, PQQ).
Inhaltsverzeichnis
Semichinone
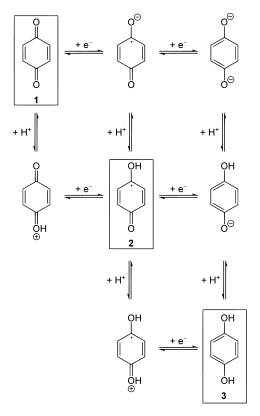 Redoxgleichgewichte (horizontal) sowie Säure-Basen-Gleichgewichte (vertikal) für Chinon an Beispiel von 1,4-Benzochinon.[1]
Redoxgleichgewichte (horizontal) sowie Säure-Basen-Gleichgewichte (vertikal) für Chinon an Beispiel von 1,4-Benzochinon.[1]Die Reduktion von Chinonen zu Chinolen geschieht mehrstufig über reaktive radikalische Zwischenverbindungen, die Semichinone. Dabei sind die Reduktionsvorgänge mit Säure-Basen-Gleichgewichte gekoppelt.[2] Diese sind z. T. recht beständig, wie die Semichinone der Ubichinone. Die Reduktion des Chinons mit der Bildung eines Semichinons und dessen weiterführende Reduktion zum Hydrochinon sei am Beispiel von 1,4-Benzochinon erläutert:
Aus dem 1,4-Benzochinon 1 entsteht nach Protonierung und Reduktion das Semichinon 2. Das ungepaarte Elektron ist dabei über das semichinoide System verteilt. Die weitere Reduktion nebst Protonierung führt zum Hydrochinon 3.
Herstellung
Chinone bilden sich u. a. durch Oxidation von Phenolen oder polycyclischen aromatischen Kohlenwasserstoffen. Dabei erweisen sich besonders Cer(IV)-Verbindungen (Cerammoniumnitrat) als nützlich.
Reaktionen
Synthetisch wichtig sind die (gegebenenfalls photochemisch ausgelösten) Cycloadditions-Reaktionen der Chinone, die zu Cyclobutan-Derivaten, Oxetanen, Käfigverbindungen und Pyranen führen können. Olefine addieren sich z. B. bei Belichtung an das 1,2-Dicarbonyl-System von ortho-Chinonen, das in diesen Fällen als Hetero-1,3-dien-System fungiert (siehe Diels-Alder-Reaktion). Dies geschieht unter anderem unter Bildung von Dioxan-Derivaten (Schönberg-Reaktion).
Das im Gegensatz zu den Reinsubstanzen tieffarbige 1:1-Gemisch von 1,4-Hydrochinon und 1,4-Benzochinon nennt man Chinhydron, ein klassisches Beispiel für einen Charge-Transfer-Komplex.
Vorkommen
In der Natur kommen Chinone besonders häufig in Farbstoffen vor, z. B. in Pilzen, Bakterien oder Blüten. Chinoide Systeme findet man auch in verschiedenen Antibiotika. Chinone entstehen auch durch enzymatische Oxidation von Polyphenolen. So spielen Chinone beispielsweise bei der Braunfärbung angeschnittener Äpfel eine wichtige Rolle.
Bekannte Chinone sind:
- die Ubichinone als Elektronenüberträger in der Atmungskette
- die Plastochinone bei der Photosynthese
- die K-Vitamine (Phyllochinon, Menachinon)
- das Pyrrolochinolinchinon (PQQ)
- das Tryptophantryptophylchinon (TQQ)
- das Dichlordicyanochinon (DDQ)
- die Hydroxynaphthochinone (in Henna und Walnüssen)
- Echinochrom A, Adrenochrom, Dopachrom
Chinone werden auch in den Wehrsekreten von Insekten gefunden, vor allem Benzo- und Toluchinone.
Verwendung
Chinone finden als Oxidationsmittel, Bakterizide und analytische Reagenzien Verwendung. Sie entstehen auch als Zwischenprodukt bei Farbstoffsynthesen (siehe auch Alizarin). Auch in Malariamedikamenten spielen Chinone eine wichtige Rolle. In der technischen Chemie sind sie vor allem zur Gewinnung von Wasserstoffperoxid über Anthrachinon wichtig.
Quellen
- ↑ nach Paul Rys und Heinrich Zollinger: Farbstoffchemie. Ein Leitfaden. Wiley-VCH; 3. neubearb. Auflage 1982; ISBN 3-527-25964-3; S.45
- ↑ Michaelis, L. und Schubert, MP. (1938): The Theory of Reversible Two-step Oxidation Involving Free Radicals. In: Chem. Reviews 22(3); 437–470; doi:10.1021/cr60073a003
Wikimedia Foundation.