- Chitin
-
Strukturformel 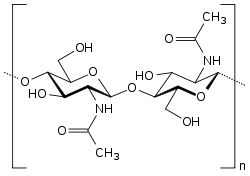
Allgemeines Name Chitin CAS-Nummer 1398-61-4 Art des Polymers Biopolymer Kurzbeschreibung Polysaccharid, weißlicher, geruchloser Feststoff[1] Monomer Monomer Acetylglucosamin Summenformel C8H13NO5 Molare Masse 203,19 g·mol−1 Eigenschaften Aggregatzustand fest Löslichkeit in Wasser und organischen Lösungsmitteln praktisch unlöslich, mäßige bis geringe Löslichkeit in wasserfreier Ameisensäure.
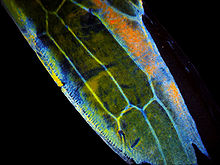
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Chitin (gr. χιτών chitón „Hülle“, „Panzer“) ist neben Zellulose das am weitesten verbreitete Polysaccharid auf der Erde und dient der Strukturbildung. Es unterscheidet sich von Zellulose durch eine Acetamidgruppe. Es kommt sowohl bei Pilzen (Fungi) als auch bei Gliedertieren (Articulata) und Weichtieren (Mollusca) vor. Bei Pilzen bildet es einen der Hauptbestandteile der Zellwand. Bei Ringelwürmern (Annelida) kommt es im Mundraum vor. Bei Gliederfüßern (Arthropoden) ist es Hauptbestandteil des Exoskeletts. Auch bei Wirbeltieren wurde es gefunden, etwa bei Knochenfischen (Teleostei) und Schleimfischen (Blenniidae) wie dem Grauen Schleimfisch (Paralipophrys trigloides).[2] Das Chitin der Gliederfüßer kommt hauptsächlich in Form von α-Chitin vor, bei Weichtieren in Form des β-Chitins.
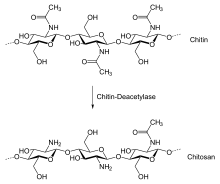
Chitin ist Ausgangsstoff für die technische Herstellung von Chitosan und Glucosamin.
Inhaltsverzeichnis
Vorkommen
Im Tierreich hat Chitin, in Verbindung mit Protein und Calciumcarbonat, die größte Verbreitung als Bestandteil im Exoskelett vieler Arthropoda, vor allem der Klassen (bzw. Überklassen) der Insecta, Arachnida (Spinnentiere), Myriapoda (Tausendfüßer) und Crustacea (Krebstiere). Bei den Mollusca (Weichtiere) ist es als Bestandteil der Radula sowie im Schulp mancher Cephalopoda (Kopffüsser) zu finden.
Im Pilzreich findet man Chitin in einer Reihe niederer Pilze sowie bei Basidiomyceten, Ascomyceten und Schlauchpilzen (Phycomyceten) als Zellwandkomponente mit Proteinen und Glucanen, wobei es nicht in allen dieser Pilze vorkommt. Auch bei engen Verwandten kann sich das Vorkommen von Chitin in der Zellwand erheblich unterscheiden.
Eigenschaften
Chitin ist ein Polysaccharid, das aus Acetylglucosamin-Einheiten aufgebaut ist (präzise: 2-Acetamido-2-desoxy-D-glucopyranose, kurz: N-Acetyl-D-glucosamin, Abkürzung: GlcNAc). Die Acetylglucosamin-Einheiten sind durch β-1,4-glycosidische Bindungen verknüpft – dies ist die gleiche Bindungsart wie die der Glucosemoleküle in Cellulose. Chitin kann also als Abart der Cellulose aufgefasst werden, bei der die Hydroxygruppen in Position 2 der Monomereinheiten durch Acetamidogruppen ersetzt wurde. Dadurch wird eine stärkere Wasserstoffbrückenbindung zwischen angrenzenden Polymeren ermöglicht, die Chitin härter und stabiler als Cellulose macht.[3] Natürliches Chitin ist jedoch meist kein einheitliches Polymer, sondern eine Mischung statistischer Copolymere aus D-Glucosamin (GlcN) und N-Acetyl-D-glucosamin (GlcNAc), das heißt, nicht jede Aminogruppe ist acetyliert. Der Grad der Acetylierung bestimmt seine Eigenschaften zusätzlich zum Polymerisationsgrad (Kettenlänge) und der Kettenfaltung. Der Übergang zum Chitosan, welches deutlich weniger (im Idealfall gar keine) Acetylgruppen trägt, ist daher fließend. Ist der Acetylierungsgrad höher als 50%, so spricht man meist von Chitin, liegt er darunter, ist es Chitosan.
Farbe: Chitin ist farblos. Die bekannte Braunfärbung des Insektenpanzers rührt von dem eingelagerten Protein Sklerotin bzw. dessen Vorstufe Prosklerotin bzw. des daraus resultierenden verfestigten Arthropodins her.
Löslichkeit: Chitin ist in wässrigen, schwach ionischen und gesundheitlich tolerierbaren organischen Lösungsmitteln weitgehend unlöslich, in stark ionischen beruht die „Löslichkeit“ auf einer Depolymerisation. Bei „löslichem Chitin“ handelt es sich meist um Chitin-Hydrochloride, die teilweise sogar in Wasser löslich sind.[4]
Biosynthese
Chitin bildet in der Natur komplexe Strukturen, die in einem mehrstufigen Prozess gebildet werden. Die Synthese von Chitinmolekülen erfolgt durch Transglycosylierungen durch, als Chitinsynthetase EC 2.4.1.16 bezeichnete, Membran-gebundene Enzyme, die Uridindiphosphat-N-acetylglucosamin (UDPGlcNAc) als Substrat verwenden. Bei Pilzen geschieht dies beispielsweise in speziellen Vesikeln, die als Chitosomen bezeichnet werden. Die Chitinmoleküle oder Chito-Oligomere werden in Extrazellularraum sekretiert. Außerhalb der Zellen finden verschiedene Modifikationen statt, die die Eigenschaften beeinflussen. Eine davon ist die partielle Hydrolyse durch Chitinasen EC 3.2.1.14. Chitinasen haben neben der Hydrolase auch eine Transglycosidase-Aktivität, so dass Chitin mit Glucanen verknüpft werden kann. Eine weitere Modifikation ist die teilweise Deacetylierung durch spezielle Deacetylasen. Einige unmodifizierte Chitinmoleküle kristallisieren und werden mit weiteren Chitinmolekülen über Proteine teilweise kovalent vernetzt. Die entstehende supramolekulare Struktur reift durch weitere Quervernetzung und die Einlagerung verschiedener Substanzen.[5]
Biologische Bedeutung
Entgegen der landläufigen Meinung ist Chitin nicht dafür verantwortlich, dass ein (Insekten-) Panzer hart ist. Chitin ist für dessen Weichheit und Biegsamkeit verantwortlich. Erst im Zusammenspiel mit dem Strukturprotein Sklerotin wird die Cuticula der Insekten hart und stabil. Bei Crustaceen wird zur Erhöhung der Härte zusätzlich Kalk eingelagert.
Chitin ist das zweithäufigste Biopolymer nach der Cellulose. Der Weltvorrat wird auf 106 bis 107 Tonnen geschätzt. Den Hauptanteil machen dabei die Kleinkrebse des Zooplanktons (z.B. Krill) aus.
Chitin von aquatisch lebenden Gliedertieren und Pilzen wird u. a. von Vibrio cholerae, dem Choleraerreger, mit Hilfe des Enzyms Chitinase abgebaut.
Wirkstoffe, die die Chitinsynthese hemmen, werden als Chitininhibitoren bezeichnet und zur Bekämpfung von Insekten und Pilzen eingesetzt.
Geschichte der Entdeckung
Chitin wurde 1811 von Henri Braconnot (Direktor des Botanischen Gartens von Nancy) erstmalig wissenschaftlich als Substanz (aus Pilzen) beschrieben, allerdings noch nicht unter dieser Bezeichnung, sondern als „Fungin“. Der Franzose Antoine Odier war 1823 namensgebend: er nahm das griechische Wort für „Tunika“ oder „Ummantelung“, in Anlehnung an die Flügeldecken des Maikäfers, in welchen er die Substanz gefunden hatte.[6]
Medizinische Bedeutung
Chitin ist auch Bestandteil wichtiger Krankheitserreger; es wird in den Zellwänden pathogener Pilze, in der Scheide und dem Pharynx von Filarien sowie in den Eiern parasitischer Würmer gefunden. Säugetiere und Pflanzen verfügen zur Abwehr über Chitin abbauende Chitinasen. Bei Patienten mit Morbus Gaucher[7] finden sich extrem erhöhte Enzymwerte, welche zur Therapiekontrolle herangezogen werden. Auch bei anderen lysosomalen Speicherkrankheiten sowie Patienten mit Sarkoidose[8] finden sich erhöhte Enzymspiegel im Blut. Bei schwerem Asthma sind in Serum und Lungengewebe erhöhte Chitinasewerte nachweisbar. [9]
Nutzung
Obwohl Chitin als Biopolymer sehr gute mechanische Eigenschaften hat und neben Cellulose und Lignin eines der häufigsten Naturpolymere darstellt, ist das Nutzungsspektrum vergleichsweise gering. Das vom Chitin abgeleitete Chitosan wird kommerziell aus Schalenresten von Garnelen hergestellt und vor allem als Fettblocker im Ernährungsbereich sowie als Filtermaterial zur Wassergewinnung oder in Kläranlagen sowie als Ausgangsmaterial für Fasern, Schaumstoffe, Membranen und Folien (Biokunststoff) verwendet. Des Weiteren findet Chitosan Verwendung in Zahnpasten (Chitodent), als Papier- und Baumwollzusatz sowie zum Ausfällen von Trübungen in der Getränkemittelindustrie. In der Arzneimittelindustrie wird an Chitosan geforscht, um es zur Mikroverkapselung und gezielten Freisetzung pharmakologischer Wirkstoffe zu verwenden, unter anderem als Vektor für die Gentherapie.
Chitin ist außerdem Ausgangsstoff für die technische Herstellung von Glucosamin, einem natürlichen Bestandteil des Knorpels und der Gelenkflüssigkeit (Synovialflüssigkeit). Technisch hergestelltes Glucosamin findet Verwendung in der Arzneimittelindustrie u.a. in Mitteln gegen Arthrose.
Einzelnachweise
- ↑ Datenblatt Chitin bei Carl Roth, abgerufen am 14. Dezember 2010.
- ↑ G. P. Wagner, J. Lo, R. Laine, M. Almeder: Chitin in the epidermal cuticle of a vertebrate (Paralipophrys trigloides, Blenniidae, Teleostei). Experentia. 49:317-319 (1993).
- ↑ Chitin
- ↑ ChemieOnline: Chitin/Chitosan [1]
- ↑ J. Ruiz-Herrera und A. D. Martínez-Espinoza: Chitin biosynthesis and structural organization in vivo. In: EXS Band 87, 1999, S. 39–53, ISSN 1023-294X. PMID 10906950. (Review).
- ↑ Daniel Essmann, Bengt Neumann und Tobias Voß: Chitin und Chitosan Hausarbeit im Rahmen der Vorlesung Bionik, WS 2005-2006, Universität Bremen, unter Anleitung von Prof. Dr. Arnim von Gleich entstanden
- ↑ Guo Yufeng et al. (1995): Elevated plasma chitotriosidase activity in various lysosomal storage disorders. In: Journal of inherited metabolic disease, PMID 8750610
- ↑ Grosso, Bargagli et al. (2004): Serum levels of chitotriosidase as a marker of disease activity and clinical stage in sarcoidosis. In: Scandinavian Journal of Clinical and Laboratory Investigation 2004;64(1):57-62, PMID 15025429
- ↑ Chupp, Geoffrey L. et al.: A Chitinase-like Protein in the Lung and Circulation of Patients with Severe Asthma. In: N Engl J Med. Nr. 357, 2007, S. 2016-2027 (Abstract).
Weblinks
- www.wissenschaft.de: Unerwartetes Allergiepotenzial – Studie: Biopolymer Chitin ruft allergieähnliche Entzündungen hervor (Zusammenfassung eines Artikels aus Nature: Tiffany A. Reese, Hong-Erh Liang, Andrew M. Tager, Andrew D. Luster, Nico Van Rooijen, David Voehringer, Richard M. Locksley. Chitin induces accumulation in tissue of innate immune cells associated with allergy. Nature advance online publication 22 April 2007)
- Sachanalyse Chitin / Chitosan
- Informationen über Chitin (Heppe Medical Chitosan)
Wikimedia Foundation.