- Glycidamid
-
Strukturformel 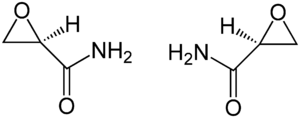
(R)-Enantiomer (links) und (S)-Enantiomer (rechts) Allgemeines Name Glycidamid Andere Namen - (±)-2,3-Epoxypropanamid
- (±)-Glycidamid
- (RS)-Glycidamid
- (R)-Glycidamid
- (S)-Glycidamid
Summenformel C3H5NO2 CAS-Nummer 5694-00-8 (Racemat) PubChem 91550 Kurzbeschreibung hellorange Kristalle[1]
Eigenschaften Molare Masse 87,08 g·mol−1 Dichte 1,39 g·cm−1[2]
Schmelzpunkt 32 − 34 °C[1]
Siedepunkt Dampfdruck Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [1] 

Gefahr
H- und P-Sätze H: 302-315-317-319-335-350 EUH: keine EUH-Sätze P: 201-261-280-305+351+338-308+313 [1] EU-Gefahrstoffkennzeichnung [1] 
Giftig (T) R- und S-Sätze R: 22-36/37/38-43-45-46 S: 26-36/37-45-53 MAK Für krebserzeugende Stoffe wird generell kein Wert vergeben[4]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Das Glycidamid gehört zu den chemischen Gruppen der Amide und der Oxirane. Glycidamid ist ein als stark krebserregend eingestufter Stoff, der in hoch erhitzten Lebensmitteln vorkommt.[5] Er entsteht aus Acrylamid durch Reaktion mit ungesättigten Fettsäuren und Sauerstoff, ist aber wesentlich gefährlicher als dieses, denn schon geringe Mengen können zu Mutationen in Zellen führen. Ein weiterer biologisch relevanter Syntheseweg läuft im Stoffwechsel in der Leber ab, wo Acrylamid zu Glycidamid umgewandelt wird.
Inhaltsverzeichnis
Synthese
Bei der Umsetzung von Acrylnitril mit Wasserstoffperoxid entsteht racemisches Glycidamid. Die Selektivität und Ausbeute an Glycidamid kann durch kontinuierliche Zugabe von Natronlauge zum Reaktionsgemisch gesteigert werden.[6]
Stereoisomerie
Glycidamid ist chiral. Es gibt zwei Enantiomere dieser Verbindung: (R)-Glycidamid und das dazu spiegelbildliche (S)-Glycidamid. Das Racemat (RS)-Glycidamid ist eine 1:1-Mischung von (R)-Glycidamid und (S)-Glycidamid.
Einzelnachweise
- ↑ a b c d e Datenblatt Glycidamide bei Sigma-Aldrich, abgerufen am 3. April 2011.
- ↑ a b Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.5. Georg Thieme Verlag KG, Stuttgart 2009.
- ↑ G. B. Payne, in: J. Org. Chem. 1961, 26, 651–659.
- ↑ "Grenzwerte am Arbeitsplatz", Maximale Arbeitsplatz-Konzentrationswerte (MAK-Werte), Biologische Arbeitsstoff-Toleranzwerte (BAT-Werte) und Grenzwerte für physikalische Einwirkungen. Periodisch publiziert von SUVA.ch. PDF-Datei 2011
- ↑ M. Granvogl, P. Koehler, L. Latzer, P. Schieberle: Development of a Stable Isotope Dilution Assay for the Quantitation of Glycidamide and Its Application to Foods and Model Systems, in: Journal of Agriculture and Food Chemistry 2008, 56, 6087–6092.
- ↑ S. Sugiyama, S. Ohigashi, R. Sawa, H. Hayashi: Selective preparation of 2,3-epoxypropanamide and its facile conversion to 2,3-dihydroxypropanamide with acidic resins, in: Bull. Chem. Soc. Jpn. 1989, 62, 3202–3206.
Weblinks
Kategorien:- Gesundheitsschädlicher Stoff
- Sensibilisierender Stoff
- Krebserzeugender Stoff
- Erbgutverändernder Stoff
- Epoxid
- Carbonsäureamid
Wikimedia Foundation.
