- Nickel(II)-chlorid
-
Strukturformel 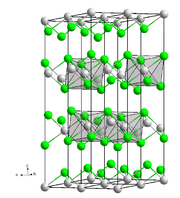
__ Ni2+ __ Cl− Allgemeines Name Nickel(II)-chlorid Andere Namen - Nickeldichlorid
- Nickelchlorid
Summenformel - NiCl2 (wasserfrei)
- NiCl2 · 6 H2O (Hexahydrat)
CAS-Nummer - 7718-54-9 (wasserfrei)
- 7791-20-0 (Hexahydrat)
Kurzbeschreibung Eigenschaften Molare Masse Aggregatzustand fest
Dichte Schmelzpunkt Dampfdruck Löslichkeit sehr gut in Wasser (2540 g·l−1, Hexahydrat bei 20 °C)[1]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [2] 


Gefahr
H- und P-Sätze H: 350i-341-360D-331-301-372-315-334-317-410 EUH: keine EUH-Sätze P: 273-281-302+352-304+340-309+310 [1] EU-Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 49-61-23/25-38-42/43-48/23-68-50/53 S: 53-45-60-61 MAK keine Einstufung, da krebserzeugend[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Nickel(II)-chlorid, NiCl2, ist das Nickel-Salz der Salzsäure.
Es bildet gelbe, in Wasser und Ethanol gut lösliche Kristalle. Neben der wasserfreien Form (NiCl2, Anhydrat), existiert das wasserhaltige Nickel(II)-chlorid-hexahydrat, NiCl2 · 6 H2O, welches grüne Kristalle ausbildet. Weiterhin ist das Nickel(II)-chlorid-dihydrat, NiCl2 · 2 H2O, bekannt.
Inhaltsverzeichnis
Eigenschaften
Das wasserfreie Nickel(II)-chlorid-Anhydrat ist ein stark hygroskopisches Salz. Es hat eine CdCl2-Struktur.[3] Im Gegensatz dazu besitzt Nickel(II)-chlorid-hexahydrat eine ähnliche Struktur wie auch Cobalt(II)-chlorid-Hexahydrat und besteht aus einzelnen trans-[NiCl2(H2O)4] Molekülen mit schwacher Bindung zu den benachbarten Wassermolekülen. Dabei sind nur vier der sechs Wasser-Moleküle aus der Formel mit dem die Nickel verbunden. Die restlichen zwei sind Kristallwasser.[3] Das Hexahydrat kristallisiert im monoklinen Kristallsystem in der Raumgruppe C2h3--C2/m mit den Gitterparametern a = 1023 pm, b = 705 pm, c = 657 pm und β = 122,17°. In der Elementarzelle befinden sich zwei Formeleinheiten.[4]
Nickel(II)-chlorid ist wasserlöslich, leicht resorbierbar und giftig. Die LD50 bei Ratten ist 681 mg/kg[5] bzw. 105 mg/kg.[6] Die Kanzerogenität (Krebsauslösung) gilt ebenfalls als erwiesen. Außerdem besteht bei allen Nickelverbindungen die Gefahr der Sensibilisierung (Allergisierung).
Herstellung
Das grüne Nickel(II)-chlorid-hexahydrat NiCl2 · 6 H2O kristallisiert durch Umsetzung von Salzsäure (HCl) mit Nickelhydroxid Ni(OH)2 aus wässrigen Lösungen aus. Es bildet dabei typischerweise monokline Prismen als Kristallform.
Gelbes, wasserfreies NiCl2 lässt sich durch Trocknung im Chlorwasserstoff-Strom bei einer Temperatur von ca. 140 °C oder Erhitzung in Thionylchlorid aus dem Hexahydrat gewinnen.Die Entwässerung wird durch den Wechsel der Farbe von grün nach gelb angezeigt. Die Herstellung der wasserfreien Form kann auch aus elementarem Nickel durch längere Einwirkung von HCl bei Temperaturen oberhalb 550 °C erfolgen.
Verwendung
Es dient als Farbstoff in der Keramik, in der galvanischen Vernickelung und zur Herstellung von Nickelkatalysatoren. Nickel(II)-chlorid ist weiterhin ein möglicher Nickelelektrolyt zur Vernickelung metallischer Oberflächen und ein Beizmittel in der Färberei. Die wasserfreie Form wird als Absorber für Ammoniak in Gasmaskenfiltern eingesetzt.
Einzelnachweise
- ↑ a b c d e f g h i Eintrag zu CAS-Nr. 7718-54-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 12. Januar 2008 (JavaScript erforderlich).
- ↑ a b Eintrag zu CAS-Nr. 7718-54-9 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ a b A. F. Wells: Structural Inorganic Chemistry, Oxford Press, Oxford, Vereinigtes Königreich, 1984.
- ↑ J. Mizuno: "The Crystal Structure of Nickel Chloride Hexahydrate, NiCl2 · 6 H2O", in: Journal of the Physical Society of Japan, 1961, 16 (8), S. 1574. Abstract
- ↑ Indian Journal of Pharmacology, 1991, Vol. 23, S. 153.
- ↑ Russian Pharmacology and Toxicology, 1969, Vol. 32, S. 102.
NickelhalogenideOxidationsstufe (II): Nickel(II)-fluorid | Nickel(II)-chlorid | Nickel(II)-bromid | Nickel(II)-iodid
Andere Oxidationsstufen: Nickel(III)-fluorid | Nickel(IV)-fluorid
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Nickel(II)chlorid — Strukturformel Ni2+ Cl … Deutsch Wikipedia
Nickel — Eigenschaften … Deutsch Wikipedia
Nickel(II)-fluorid — Kristallstruktur Ni2+ … Deutsch Wikipedia
Nickel(II)-iodid — Kristallstruktur Ni2+ … Deutsch Wikipedia
Nickel(II)-hydroxid — Kristallstruktur Ni2+ … Deutsch Wikipedia
Nickel(II)-bromid — Kristallstruktur Ni2+ … Deutsch Wikipedia
Nickel(II)-sulfat — Strukturformel Allgemeines Name … Deutsch Wikipedia
Nickel(II)-carbonat — Strukturformel Allgemeines Name Nickel(II) carbonat Andere Name … Deutsch Wikipedia
Nickel(III)-oxid — Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Nickel(III) oxid Andere Namen Nickelsesquioxid Dinickeltrioxid Nickeloxid (Achtung: mehrdeutig) Nickeloxid (schwarz) … Deutsch Wikipedia
Zink-Chlorid-Batterie — Die Zinkchlorid Batterie ist eine Batterie spezieller Bauart. Dieser Typ gehörte bis zum Ende der 1970er Jahre zu den meist benutzten Batterietypen. Heute wird sie für Taschenlampen, Spielzeug und elektrische Kleingeräte verwendet. Die… … Deutsch Wikipedia


