- Titan(IV)-chlorid
-
Strukturformel 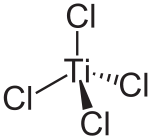
Allgemeines Name Titan(IV)-chlorid Andere Namen Titantetrachlorid
Summenformel TiCl4 CAS-Nummer 7550-45-0 Kurzbeschreibung farblose, stechend riechende, an feuchter Luft stark rauchende Flüssigkeit[1]
Eigenschaften Molare Masse 189,71 g·mol−1 Aggregatzustand flüssig
Dichte 1,73 g·cm−3[2]
Schmelzpunkt Siedepunkt 136,5 °C[2]
Dampfdruck Löslichkeit Sicherheitshinweise GHS-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 
Gefahr
H- und P-Sätze H: 314 EUH: 014 P: 280-305+351+338-310 [4] EU-Gefahrstoffkennzeichnung aus EU-Verordnung (EG) 1272/2008 (CLP) [3] 
Ätzend (C) R- und S-Sätze R: 14-34 S: (1/2)-7/8-26-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Titan(IV)-chlorid (Titantetrachlorid) ist eine chemische Verbindung aus Chlor und Titan. Das Titan liegt in TiCl4 in seiner höchsten und stabilsten Oxidationsstufe vor.
Es sind weitere Chlorverbindungen des Titans, darunter beispielsweise Titan(III)-chlorid, das ein starkes Reduktionsmittel ist, bekannt.[5]
Inhaltsverzeichnis
Herstellung
Titantetrachlorid wird durch Carbochlorierung von Titandioxid in Gegenwart von Kohle und Chlor bei 700–1000 °C hergestellt:[1]
Es ist ein Zwischenprodukt des Kroll-Prozesses zur Herstellung von Titan.
Verwendung
Titantetrachlorid ist eine wichtige Lewissäure und wird in der Organischen Chemie in Knoevenagel-Reaktionen und der Mukaiyama-Michael-Reaktion verwendet. Es ist zudem Grundstoff für Katalysatoren, wie beispielsweise Ziegler-Natta-Katalysatoren, und Ausgangsstoff für Organo-Titan-Verbindungen. Titantetrachlorid findet in Raucherzeugern für militärische Zwecke Verwendung (vergleiche: Nebelkampfstoff). Das Titantetrachlorid wird heute überwiegend im „Chloridverfahren“ durch Sauerstoff oder Luft zu Titandioxid umgesetzt. Es wird auch in der nass-analytischen Chemie zum Nachweis von Peroxiden benutzt. Bei Peroxidanwesenheit verfärbt sich die Lösung gelblich bis orange.
Eigenschaften
Titantetrachlorid hydrolysiert mit Wasser in einer heftigen Reaktion zu Titandioxid (Rauch) und Chlorwasserstoff (korrosiv). Bereits bei Kontakt mit Luftfeuchtigkeit findet die Hydrolyse statt.
Wirkung im Körper
Besonders beim militärischen Einsatz als Nebelkampfstoff besteht die Gefahr des Einatmens des entstehenden Chlorwasserstoffes HCl. Dieses kann zu Reizungen oder sogar Verätzungen der Schleimhäute oder des Lungengewebes führen. Erste Symptome beim Einatmen sind Husten und Brustschmerzen. Dauern die Symptome länger als 20 Minuten, ist mit einem lebensbedrohlichem Lungenödem zu rechnen, welches auch ohne anhaltende Symptome auftreten kann.
Einzelnachweise
- ↑ a b c d Römpp Online - Version 3.5, 2009, Georg Thieme Verlag, Stuttgart.
- ↑ a b c d Eintrag zu Titan(IV)-chlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 5.12.2007 (JavaScript erforderlich)
- ↑ a b Eintrag zu CAS-Nr. 7550-45-0 im European chemical Substances Information System ESIS (ergänzender Eintrag)
- ↑ Datenblatt Titanium(IV) chloride bei Sigma-Aldrich, abgerufen am 24. April 2011.
- ↑ Zur Bestimmung von Titandichlorid und -trichlorid in Alkali- oder Erdalkalichloridschmelzen, in Fresenius' Journal of Analytical Chemistry, 171/1959, S. 151–152
Weblinks
 Commons: Titan(IV)-chlorid – Sammlung von Bildern, Videos und AudiodateienTitanhalogenide
Commons: Titan(IV)-chlorid – Sammlung von Bildern, Videos und AudiodateienTitanhalogenideOxidationsstufe (II): Titan(II)-chlorid | Titan(II)-bromid | Titan(II)-iodid
Oxidationsstufe (III): Titan(III)-fluorid | Titan(III)-chlorid | Titan(III)-bromid | Titan(III)-iodid
Oxidationsstufe (IV): Titan(IV)-fluorid | Titan(IV)-chlorid | Titan(IV)-bromid | Titan(V)-fluorid
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Titan(III)-chlorid — Kristallstruktur Ti3+ … Deutsch Wikipedia
Titan(II)-chlorid — Kristallstruktur Ti2+ … Deutsch Wikipedia
Titan (Element) — Eigenschaften … Deutsch Wikipedia
Titan(III)-fluorid — Kristallstruktur Allgemeines Name Titan(III) fluorid … Deutsch Wikipedia
Titan [2] — Titan, chemisches Zeichen Ti, Atomgewicht 25 (H = 1) od. 312,5 (O = 100), ein ziemlich seltenes Metall, wurde 1791 von einem englischen Geistlichen, Gregor, im Menakan u. 1794 von Klaproth im Rutil entdeckt. Es findet sich niemals frei in der… … Pierer's Universal-Lexikon
Tetrakis(dimethylamino)titan — Strukturformel Allgemeines Name Tetrakis(dimethylamino)titan Andere Namen TDMAT … Deutsch Wikipedia
Yttrium(III)-chlorid — Kristallstruktur Y3+ … Deutsch Wikipedia
Chemikalienliste — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Liste chemischer Verbindungen — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia
Liste von chemischen Verbindungen — Die Chemikalienliste stellt eine alphabetisch sortierte Liste von Chemikalien dar, ohne Anspruch auf Vollständigkeit. Elemente sind fett gekennzeichnet, Stoffgruppen kursiv. Der Haupteintrag zu einer Chemikalie ist gleichzeitig der Name des… … Deutsch Wikipedia

