- Trimethylsilyliodid
-
Strukturformel 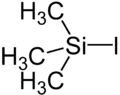
Allgemeines Name Trimethylsilyliodid Andere Namen Iodtrimethylsilan
Summenformel C3H9ISi CAS-Nummer 16029-98-4 Kurzbeschreibung orangefarbene bis bräunliche Flüssigkeit mit stechendem Geruch[1]
Eigenschaften Molare Masse 200,09 g·mol−1 Aggregatzustand flüssig
Dichte 1,47 g·cm−3[1]
Siedepunkt Löslichkeit Zersetzung mit Wasser[1]
Brechungsindex 1,471[2]
Sicherheitshinweise GHS-Gefahrstoffkennzeichnung [2] 

Gefahr
H- und P-Sätze H: 225-314 EUH: keine EUH-Sätze P: 210-280-305+351+338-310 [2] EU-Gefahrstoffkennzeichnung [1] 

Leicht-
entzündlichÄtzend (F) (C) R- und S-Sätze R: 11-14-34 S: 7/9-16-26-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C Trimethylsilyliodid ist eine chemische Verbindung. Sie besteht aus einem zentralen Siliciumatom, das nahezu tetraedrisch von drei Methylresten und einem Iodsubstituenten umgeben ist.
Inhaltsverzeichnis
Herstellung
Trimethylsilyliodid kann in einer Finkelstein-ähnlichen Reaktion durch die Umsetzung von Trimethylsilylchlorid mit Natriumiodid[3] oder Magnesiumiodid[4] erhalten werden.
Eine weitere Möglichkeit besteht in der Spaltung von Hexamethyldisilan[5] oder Hexamethyldisiloxan[6] durch Iod.
Eigenschaften
Trimethylsilyliodid ist eine orangefarbene bis bräunliche Flüssigkeit, die bei 107 °C siedet.
Verwendung
Trimethylsilyliodid kann zur Synthese von Eschenmosersalz genutzt werden. Hierzu wird es mit Tetra-N-methylmethandiamin zur Reaktion gebracht.[7]
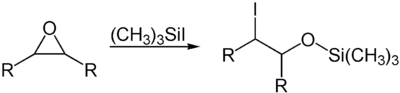
Durch seine Lewis-sauren Eigenschaften kann es auch zur Öffnung von sauerstoffhaltigen Heterocyclen genutzt werden. Ein Beispiel hierfür ist die Öffnung von Epoxiden.[8]
Einzelnachweise
- ↑ a b c d e Datenblatt Trimethylsilyliodid bei Merck, abgerufen am 27. Februar 2010..
- ↑ a b c Datenblatt Iodotrimethylsilane bei Sigma-Aldrich, abgerufen am 24. April 2011.
- ↑ C. Paolucci, L. Mattioli: Stereoisomeric Sugar-Derived Indolizines as Versatile Building Blocks: Synthesis of Enantiopure Di- and Tetrahydroxyindolizidines, in: J. Org. Chem., 2001, 66, S. 4787–4794; doi:10.1021/jo0016428.
- ↑ U. Krüerke: Halogen-Austausch an Chlorsilanen und die Tetrahydrofuran-Spaltung durch Brom-und Jodsilane, in: Chem. Ber., 1962, 95, S. 174–182; doi:10.1002/cber.19620950128.
- ↑ E. C. Friedrich, C. B. Abma, P. F. Vartanian: Metal-halogen bonding studies with group IV A trialkylmetal halides, in: J. Organomet. Chem., 1980, 187, S. 203-211; doi:10.1016/S0022-328X(00)81789-1.
- ↑ M. E. Jung, M. A. Lyster: Quantitative dealkylation of alkyl ethers via treatment with trimethylsilyl iodide. A new method for ether hydrolysis, in: J. Org. Chem., 1977, 42, S. 3761–3764; doi:10.1021/jo00443a033.
- ↑ T. A. Bryson, G. H. Bonitz, C. J. Reichel, R. E. Dardis: Performed Mannich salts: a facile preparation of dimethyl(methylene)ammonium iodide, in: J. Org. Chem., 1980, 45, S. 524–525; doi:10.1021/jo01291a032.
- ↑ H. Poleschner, M. Heydenreich, D. Martin: Cyclische Ether als Edukte zur Synthese von Schmetterlings-Pheromonen, in: Synthesis, 1991, 12, S. 1231–1235; doi:10.1055/s-1991-28425.
Wikimedia Foundation.