- Vandral
-
Strukturformel 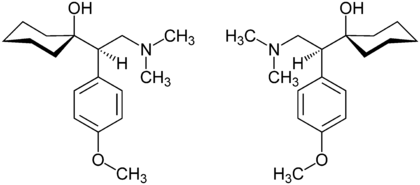
(R)-Venlafaxin (links) und (S)-Venlafaxin (rechts)
Allgemeines Freiname Venlafaxin Andere Namen Summenformel C17H27NO2 CAS-Nummer - 93413-69-5 (Venlafaxin)
- 99300-78-4 (Venlafaxin·Hydrochlorid)
PubChem 5656 ATC-Code N06AX16
DrugBank APRD00125 Kurzbeschreibung weißes bis fast weißes, polymorphes Pulver (HCl-Salz) [1] Arzneistoffangaben Wirkstoffklasse Wirkmechanismus Fertigpräparate - Efexor® (CH)
- Trevilor® (D)
- Efectin®, Efectin® ER (A)
- zahlreiche Generika
Verschreibungspflichtig: Ja Eigenschaften Molare Masse 277,40 g·mol−1 Schmelzpunkt 215–217 °C (Venlafaxin·Hydrochlorid) [2]
Löslichkeit Sicherheitshinweise Gefahrstoffkennzeichnung [3]
Venlafaxin-Hydrochlorid
Xi
ReizendR- und S-Sätze R: 36 S: 26 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Venlafaxin ist ein Phenylethylamin-Derivat und ein selektiver Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRI), der als Antidepressivum eingesetzt wird.
Inhaltsverzeichnis
Wirkprofil
Venlafaxin vermindert die Rückaufnahme (Re-Uptake) von Serotonin und Noradrenalin in die präsynaptischen Vesikel an bestimmten Synapsen im Gehirn. Das dadurch vermehrte Angebot dieser Neurotransmitter im synaptischen Spalt soll die Linderung der depressiven Symptome bewirken. Die „Muttersubstanz“ Venlafaxin (also ohne die Metaboliten, siehe unten) hat daneben noch eine schwach dopaminerge Aktivität.
Venlafaxin wird nach Einnahme in der Leber großenteils in die wirksamen Metaboliten O-Desmethyl-Venlafaxin und N-Desmethyl-Venlafaxin umgewandelt. Diese tragen zur Wirkung des Arzneistoffs bei und werden vor allem renal ausgeschieden.
Indikationen
Venlafaxin ist zur Behandlung von Depressionen zugelassen. Die Retardformulierung kann in Deutschland außerdem zur Behandlung von Angsterkrankungen wie generalisierte Angststörung und soziale Angststörung (soziale Phobie) verwendet werden. Ferner hat Venlafaxin die Zulassung zur Erhaltungstherapie und Rezidivprophylaxe depressiver Erkrankungen.
Unerwünschte Wirkungen
Zu Beginn der Einnahme treten als Nebenwirkungen oft Magen-Darm-Beschwerden auf; es kommt häufig zu vermehrter Unruhe und diffusen Angstzuständen. Psychotische Reaktionen sind beschrieben, eventuell als Folge der dopaminergen Wirkung. Vermehrte (Nacht-)Schweißbildung, Blutdruckerhöhung und Herzbeschwerden sind ebenfalls möglich. Übelkeit ist eine sehr häufige Nebenwirkung (mehr als 10 % der Patienten); unter anderem Erbrechen, Appetitlosigkeit, Verstopfung, Schwindel, Schlaflosigkeit, Nervosität, Zähneknirschen, Zittern und Sehstörungen sind häufig (1–10 % der Patienten). Weiterhin kann es zu Benommenheit und Müdigkeit kommen. Venlafaxin löst sehr häufig sexuelle Funktionsstörungen aus und kann die Libido vermindern.[4][5]
Suizidalität
Venlafaxin soll bei unter 25jährigen Anwendern die Suizidalität (Selbstmordneigung) im Vergleich zu Scheinmedikament (Plazebo) um den Faktor 5 steigern. Das geht aus einer Analyse der US-Aufsichtsbehörde FDA hervor, die alle Daten aus klinischen Studien mit Venlafaxin berücksichtigte – sowohl aus veröffentlichten und unveröffentlichten (vom Hersteller zurückgehaltenen) Untersuchungen.[6] Eine Erklärung dafür ist die von Patienten berichtete Verflachung der Gefühlstiefe, welche zur Unterdrückung der Todesangst führen kann. Eine weitere, eher von Ärzten ins Feld geführte Erklärung ist die Antriebssteigerung, welche das Medikament bewirken soll. Dies kann ihrer Meinung nach bei Patienten mit Suizidgedanken dazu führen, dass diese ihre Pläne ausführen. Denkbar ist, dass bei manchen Patienten beide Aspekte zum Tragen kommen und hierdurch die Schwelle zum Suizidentschluss soweit gesenkt wird, dass es in diesen Fällen zum Suizid kommt, weshalb Patienten mit Suizidgedanken besonders beobachtet werden sollten.
Konsequenzen
Wegen des besonderen Suizidrisikos und der im Vergleich zu anderen Antidepressiva höheren Toxizität sollte Venlafaxin nach Ansicht einiger Experten nicht mehr zur Erstbehandlung der Depression verwendet werden.[7] In Großbritannien wurde die Leitlinie zur Depressionsbehandlung überarbeitet, um den besonderen Risiken von Venlafaxin Rechnung zu tragen.[8]
Darreichungsformen
Der Originator Wyeth vertreibt seine Venlafaxin-haltigen Medikamente als Trevilor® Tabletten in der Stärke 37,5 mg und Trevilor retard® Retardkapseln in den Stärken 75 mg und 150 mg. Außerdem wird Venlafaxin in Deutschland seit Ende 2008 von zahlreichen Generika-Herstellern in verschiedenen Stärken und Darreichungsformen für die perorale Anwendung vertrieben.
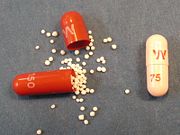
Die maximale Plasmakonzentration von Venlafaxin wird bei Tabletten nach etwa 2,4 Stunden und bei der retardierten Form nach etwa 6 Stunden erreicht. Die unretardierte Form wirkt somit früher und intensiver, was auch zu stärkeren Nebenwirkungen führt. Wegen des selteneren Auftretens der Magen-Darm-Beschwerden wird in Deutschland fast ausschließlich noch die Retardform verordnet. Die Retardkapseln sind mit etwa 5–7 mm Durchmesser und etwa 12–15 mm Länge recht groß. Außerdem enthalten sie etwas Luft, so dass sie in Wasser schwimmen.
Die Retardkapseln enthalten sogenannte Retard-Kügelchen (Retardpellets) (s. Foto), die die verzögerte Freisetzung ausmachen und welche auch nach der Entnahme aus der Kapsel erhalten bleibt.
Anwendung während der Schwangerschaft
Es liegen keine hinreichenden Daten zur Anwendung von Venlafaxin bei schwangeren Frauen vor. Bei Tierversuchen trat ein verlangsamtes Wachstum des Fötus auf. Das potentielle Risiko für den Menschen ist nicht bekannt. Venlafaxin sollte nicht während der Schwangerschaft eingesetzt werden, es sei denn, dies ist eindeutig erforderlich. Wenn Venlafaxin vor der Geburt angewendet wird, kann es beim Neugeborenen zu Entzugserscheinungen kommen. Manche Neugeborene, deren Mütter im letzten Drittel der Schwangerschaft Venlafaxin einnahmen, entwickelten Komplikationen, die Unterstützung der Atmung und verlängerten Klinikaufenthalt erforderten. Die Patientinnen sollten darauf hingewiesen werden, dass sie ihren Arzt umgehend informieren sollen, wenn sie während der Therapie mit Venlafaxin schwanger werden.[9]
Wechselwirkungen mit anderen Arzneimitteln
Unter Behandlung mit Venlafaxin kann, wie bei anderen serotonergen Wirkstoffen, ein potenziell lebenbedrohlicher Zustand, das so genannte Serotonin-Syndrom auftreten. Dies ist insbesondere dann der Fall, wenn andere Substanzen eingenommen werden, die das serotonerge Neurotransmittersystem beeinflussen können. Dazu gehören zum Beispiel Johanniskraut, Lithium, Triptane, SSRI und weitere Medikamente.[9]
Absetzsyndrom
→ Hauptartikel: SNRI Discontinuation Syndrome
Wenn die Einnahme von Venlafaxin abrupt beendet wird oder die Dosis zu schnell reduziert wird, kann es zu Absetzsymptomen kommen. Es können Anorexie, Angstgefühle, Agitiertheit, Verwirrung, Diarrhoe, Benommenheit, Mundtrockenheit, Müdigkeit, Kopfschmerzen, Hypomanie, Schlaflosigkeit oder andere Schlafstörungen, Nervosität, Parästhesie, Schläfrigkeit, Schwitzen, Schwindel, Nausea, Erbrechen, Appetitverlust, Tremor, Albträume, Schwäche, Hyperakusis, Geschmacksveränderungen, verzerrtes Sehen, Konfusion, Depersonalisation, Tinnitus, Wahnideen und verzerrte Wahrnehmung auftreten. Diese Symptome können bis zu vier Wochen nach dem Beenden der Behandlung mit Venlafaxin auftreten. Es wird aus diesem Grund empfohlen, die Behandlung ausschleichend zu beenden.[10]
Stereoisomerie
Venlafaxin ist chiral, enthält also ein Stereozentrum. Es gibt somit zwei Enantiomere, die (R)-Form und die (S)-Form. Die Handelspräparate enthalten den Arzneistoff als Racemat (1:1-Gemisch der Enantiomere), obwohl die Verwendung derartiger Racemate als Arzneistoffe umstritten ist. Die Verwendung des besser und zugleich meist nebenwirkungsärmer wirksamen Enantiomers wäre grundsätzlich zu bevorzugen.
Herstellung
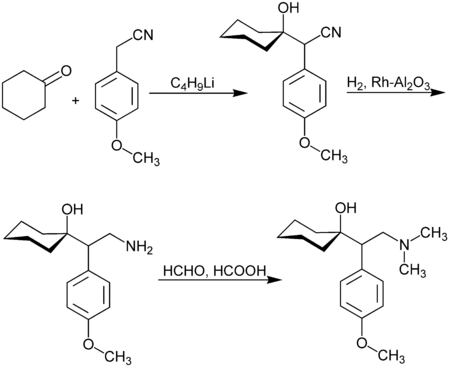
Zur Synthese von racemischem Venlafaxin geht man von Cyclohexanon und 4-Methoxyphenylacetonitril aus.[11]Einzelnachweise
- ↑ a b Europäische Arzneibuch-Kommission (Hrsg.): EUROPÄISCHE PHARMAKOPÖE 5. AUSGABE. 5.0–5.8, 2006.
- ↑ a b Thieme Chemistry (Hrsg.): RÖMPP Online - Version 3.1. Georg Thieme Verlag KG, Stuttgart 2008.
- ↑ Datenblatt für Venlafaxine hydrochloride – Sigma-Aldrich 02.01.2008
- ↑ Incidence of sexual dysfunction associated with antidepressant agents: a prospective multicenter study of 1022 outpatients. J Clin Psychiatry 2001;62 Suppl 3:10–21; PMID 11229449.
- ↑ Antidepressants and sexual dysfunction. Acta Psychiatrica Scandinavica 114 (6), 384–397.
- ↑ Clinical Review: Relationship between Antidepressant Drugs and Suicidality in Adults. FDA, 5.12.2006 (PDF, 2 MB)
- ↑ BMJ 2007;334:215.
- ↑ NICE - Consultation: Amendment to clinical guideline on depression (clinical guideline 23)
- ↑ a b Deutsche Fachinformation: Trevilor retard, Stand: Mai 2007
- ↑ Fachinformation des Arzneimittel-Kompendium der Schweiz: Efexor®/Efexor® ER; Stand der Informationen: Juli 2005
- ↑ Axel Kleemann, Jürgen Engel, Bernd Kutscher und Dietmar Reichert: Pharmaceutical Substances, 4. Auflage (2000), 2 Bände erschienen im Thieme-Verlag Stuttgart, ISBN 978-1-58890-031-9; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.
Weblinks
- pharma-kritik über Venlafaxin (Stand: 19. Juli 1996)
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.