- Everolimus
-
Strukturformel 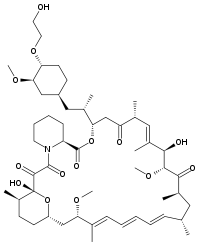
Allgemeines Freiname Everolimus Andere Namen - RAD-001
- IUPAC: Dihydroxy-12-[(2R)-1-[(1S,3R,4R)-4-(2-hydroxyethoxy)-3-methoxycyclohexyl]propan-2-yl]-19,30-dimethoxy-15,17,21,23,29,35-hexamethyl-11,36-dioxa-4-azatricyclo[30.3.1.04,9]hexatriaconta-16,24,26,28-tetraen-2,3,10,14,20-penton
Summenformel C53H83NO14 CAS-Nummer 159351-69-6 PubChem 6442177 ATC-Code DrugBank DB01590 Arzneistoffangaben Wirkstoffklasse Verschreibungspflichtig: Ja Eigenschaften Molare Masse 958,224 g•mol−1 Sicherheitshinweise Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln GHS-Gefahrstoffkennzeichnung [1] keine GHS-Piktogramme H- und P-Sätze H: keine H-Sätze EUH: keine EUH-Sätze P: keine P-Sätze EU-Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22-24/25 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Everolimus (RAD-001) ist ein Immunsuppressivum mit Makrolidstruktur (makrozyklisches Lacton) und gehört zur Medikamentenklasse der mTOR-Inhibitoren. Es wird von Novartis in der Transplantationsmedizin unter den Namen Certican® (Europa) und Zortress® (USA) und in der Onkologie unter dem Namen Afinitor® vertrieben.
Inhaltsverzeichnis
Wirkungsmechanismus
Everolimus ist ein Derivat des aus dem Streptomyzeten Streptomyces hygroscopicus isolierten Sirolimus (Rapamycin) und besitzt denselben Wirkungsmechanismus: Durch die Bildung eines Komplexes mit dem Protein mTOR („mammalian Target of Rapamycin“, deutsch etwa „Ziel des Rapamycin bei Säugetieren“), einer 282 kDa großen Phosphoinositid-3-Kinase, wird dieses inaktiviert. mTOR ist Teil der beiden Proteinkomplexe mTORC1 und mTORC2, die über verschiedene Signaltransduktionswege unter anderem die Transkription und Translation diverser Proteine und damit die Proliferation vor allem von T-Lymphozyten vorantreiben. Durch die Inhibition von mTOR werden somit sowohl die Aktivierung als auch das Voranschreiten der T-Zellen von der G1-Phase in die S-Phase des Zellzyklus verhindert.[2]
Nebenwirkungen
Die wichtigsten Nebenwirkungen von Everolimus sind Infektionen, die vor allem durch eine Myelosuppression mit daraus folgender Leukopenie bedingt sind. Daneben stehen auch Anämien und Thrombozytopenien im Vordergrund. Weitere häufige unerwünschte Wirkungen sind Wundheilungsstörungen, Pleura- und Perikardergüsse sowie erhöhte Leberenzymwerte.
Anwendungsgebiete
Everolimus wurde initial für die Second-line-Therapie beim metastasierten Nierenzellkarzinom[3] zugelassen, hat daneben inzwischen aber auch die Zulassung für die Prophylaxe einer Organabstoßung nach einer Nierentransplantation, für die Behandlung des mit der Tuberösen Sklerose assoziierten subependymalen Riesenzellastrozytoms[4] und für die Behandlung von fortgeschrittenen oder metastasierten neuroendokrinen Pankreastumoren[5] erhalten.
Derzeit laufen klinische Studien zum Einsatz bei Patienten mit Brustkrebs[6], Magenkrebs[7], Leberzellkrebs[8] und Malignen Lymphomen.[9][10] Daneben wurde über die Verwendung von Everolimus bei einer refraktären chronischen Graft-versus-Host-Reaktion berichtet.[11]
Einzelnachweise
- ↑ a b Datenblatt Everolimus bei Sigma-Aldrich, abgerufen am 4. Oktober 2011.
- ↑ Voss MH, Molina AM, Motzer RJ: mTOR inhibitors in advanced renal cell carcinoma. In: Hematol Oncol Clin North Am 25, 2011, S.835–852.
- ↑ Battelli C, Cho DC: mTOR inhibitors in renal cell carcinoma. In: Therapy 8, 2011, S. 359–367.
- ↑ Turner SG, Peters KB, Vredenburgh JJ, Desjardins A, Friedman HS, Reardon DA: Everolimus tablets for patients with subependymal giant cell astrocytoma. In: Expert Opin Pharmacother 12, 2011, S. 2265–2269.
- ↑ Kulke MH, Bendell J, Kvols L, Picus J, Pommier R, Yao J: Evolving diagnostic and treatment strategies for pancreatic neuroendocrine tumors. In: J Hematol Oncol 4, 2011, S. 1–8.
- ↑ Morrow PK, Wulf GM, Ensor J, Booser DJ, Moore JA, Flores PR, Xiong Y, Zhang S, Krop IE, Winer EP, Kindelberger DW, Coviello J, Sahin AA, Nuñez R, Hortobagyi GN, Yu D, Esteva FJ: Phase I/II study of trastuzumab in combination with everolimus (RAD001) in patients with HER2-overexpressing metastatic breast cancer who progressed on trastuzumab-based therapy. In: J Clin Oncol 29, 2011, S. 3126–3132.
- ↑ Lim T, Lee J, Lee DJ, Lee HY, Han B, Baek KK, Ahn HK, Lee SJ, Park SH, Park JO, Park YS, Lim HY, Kim KM, Kang WK: Phase I trial of capecitabine plus everolimus (RAD001) in patients with previously treated metastatic gastric cancer. In: Cancer Chemother Pharmacol 68, 2011, S. 255–262.
- ↑ Zhu AX, Abrams TA, Miksad R, Blaszkowsky LS, Meyerhardt JA, Zheng H, Muzikansky A, Clark JW, Kwak EL, Schrag D, Jors KR, Fuchs CS, Iafrate AJ, Borger DR, Ryan DP: Phase 1/2 study of everolimus in advanced hepatocellular carcinoma. In: Cancer [Epub ahead of print], 2011.
- ↑ Argyriou P, Economopoulou P, Papageorgiou S: The Role of mTOR Inhibitors for the Treatment of B-Cell Lymphomas. In: Adv Hematol 435342, 2012, S. 1–13.
- ↑ Witzig TE, Reeder CB, LaPlant BR, Gupta M, Johnston PB, Micallef IN, Porrata LF, Ansell SM, Colgan JP, Jacobsen ED, Ghobrial IM, Habermann TM: A phase II trial of the oral mTOR inhibitor everolimus in relapsed aggressive lymphoma. In: Leukemia 25, 2011, S. 341–247.
- ↑ Lutz M, Kapp M, Grigoleit GU, Stuhler G, Einsele H, Mielke S: Salvage Therapy of Refractory Chronic Graft-versus-Host Disease with Everolimus Is Associated with a Significant Reduction of Bother in the Majority of Patients. In: Onkologie 34 (Suppl. 6), 2011, S. 282.

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorien:- ATC-L01
- ATC-L04
- Arzneistoff
- Immunsuppressivum
- Enzyminhibitor
- Polyol
- Lactam
- Lacton
- Ether
- Cyclohexan
- Keton
- Polyen
- Piperidin
- Oxan
Wikimedia Foundation.
